Бикалутамид
Эта статья предлагается для быстрого удаления. |
| Бикалутамид | |
|---|---|
 | |
 | |
| Химическое соединение | |
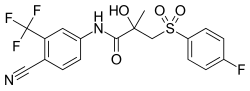
| ИЮПАК | (RS)-N-[4-cyano-3-(trifluoromethyl)phenyl]-3-[(4-fluorophenyl)sulfonyl]-2-hydroxy-2-methylpropanamide |
| Брутто-формула | C18H14F4N2O4S |
| CAS | 90357-06-5 |
| PubChem | 2375 |
| DrugBank | DB01128 |
| Состав | |
| Классификация | |
| АТХ | L02BB03 |
| Фармакокинетика | |
| Биодоступн. | хорошо всасываемый; абсолютная биодоступность неизвестна[1] |
| Связывание с белками плазмы |
Рацемат: 96.1%[2] (R)-Isomer: 99.6%[2] (в основном альбумин)[2] |
| Метаболизм |
печень (в значительной степени):[3][4] • Гидроксилирование (CYP3A4) • Глюкуронидация (UGT1A9) |
| Период полувывед. |
Однократный прием: 5-8 дней[5] Непрерывный прием: 7-10 дней[6] |
| Экскреция |
экскременты: 43%;[3] моча: 34%[3] |
| Способы введения | |
| перорально | |
Бикалутамид, продаваемый, в частности, под торговой маркой Касодекс, является антиандрогенным препаратом, который в основном используется для лечения рака предстательной железы.[7] Он обычно используется вместе с аналогом гонадотропин-рилизинг-гормона или хирургическим удалением яичек для лечения метастатического рака предстательной железы.[8][7][9] В меньшей степени он используется в высоких дозах при местнораспространенном раке предстательной железы в качестве монотерапии без кастрации.[10] Бикалутамид ранее также применялся в качестве монотерапии для лечения локализованного рака предстательной железы, но разрешение на его применение было отозвано после неблагоприятных результатов исследований.[10][11][12][13] Помимо рака предстательной железы, бикалутамид ограниченно используется для лечения чрезмерного роста волос и выпадения волос на коже головы у женщин, [14][15] в качестве блокатора полового созревания и компонента феминизирующей гормональной терапии для трансгендерных женщин, [16] для лечения гонадотропин-независимого раннего полового созревания у мальчиков,[17] и для предотвращения чрезмерно длительной эрекции у мужчин.[18] Его принимают внутрь.[7]
Распространенные побочные эффекты бикалутамида у мужчин включают увеличение груди, болезненность молочных желез и приливы жара.[7]Другие побочные эффекты у мужчин включают феминизацию и сексуальную дисфункцию.[19][20] Некоторые побочные эффекты, такие как изменение формы груди и феминизация, минимальны в сочетании с кастрацией.[21] Хотя у женщин этот препарат, по-видимому, вызывает мало побочных эффектов, в настоящее время его применение у женщин явно не одобрено Управлением по контролю за продуктами и лекарствами (FDA).[22][7] Использование во время беременности может нанести вред ребенку.[7] Было обнаружено, что у мужчин с ранним раком предстательной железы монотерапия бикалутамидом увеличивает вероятность смерти от других причин, помимо рака предстательной железы.[23][10] Бикалутамид вызывает патологические изменения в печени, которые требуют прекращения приема примерно у 1% людей.[24][10] В редких случаях это было связано со случаями серьезного повреждения печени, [7] серьезной токсичности легких, [1] и повышенной чувствительности к свету.[25][26] Хотя риск неблагоприятных изменений в печени невелик, во время лечения рекомендуется контролировать функцию печени.[7]
Бикалутамид относится к группе нестероидных антиандрогенных препаратов.[1] Он работает путем избирательного блокирования рецептора андрогена, биологической мишени андрогенных половых гормонов тестостерона и дигидротестостерона (ДГТ).[27] Он не снижает уровень андрогенов.[1] Препарат может оказывать некоторые эстрогеноподобные эффекты у мужчин при использовании в качестве монотерапии из-за повышения уровня эстрадиола.[28][29][30] Бикалутамид хорошо усваивается, и пища не влияет на его всасывание. Период полувыведения препарата составляет около одной недели.[7] У животных он проявляет периферическую избирательность, но проникает через гематоэнцефалический барьер и затрагивает как тело, так и мозг человека.[31]
Бикалутамид был запатентован в 1982 году и одобрен для медицинского применения в 1995 году.[32] Он входит в список основных лекарственных средств Всемирной организации здравоохранения.[33] Бикалутамид выпускается в виде дженериков.[34] Препарат продается более чем в 80 странах, включая большинство развитых.[35][36][37] Когда-то это был наиболее широко используемый антиандроген для лечения рака предстательной железы, и его назначали миллионам мужчин с этим заболеванием.[20][38][39][40][41] Хотя бикалутамид также используется по другим показаниям, помимо рака предстательной железы, подавляющее большинство рецептов, по-видимому, предназначено для лечения рака предстательной железы[41]
Медицинское применение[править | править код]
Бикалутамид одобрен и в основном используется при следующих показаниях:[42]
- Метастатический рак предстательной железы у мужчин в сочетании с аналогом гонадотропин-рилизинг гормона (ГнРГ) или хирургической кастрацией в дозе 50 мг/сут[24][43]
- Местнораспространенный рак предстательной железы у мужчин в качестве монотерапии в дозе 150 мг/сут (не одобрен для применения в Соединенных Штатах)[10][44]
В Японии бикалутамид используется исключительно в дозировке 80 мг/сут как в комбинации с кастрацией, так и в качестве монотерапии при лечении рака предстательной железы.[45][46]
- Для уменьшения последствий повышения уровня тестостерона в начале терапии агонистами ГнРГ у мужчин[47][48]
- Андрогензависимые заболевания кожи и волос, такие как акне, себорея, чрезмерный рост волос и выпадение волос на голове у женщин, а также высокий уровень тестостерона из-за синдрома поликистозных яичников (СПКЯ) у женщин, в дозе от 25 до 50 мг/сут, как правило, в сочетании с противозачаточными таблетками[14][49][50][51][52][53][54]
- Феминизирующая гормональная терапия для трансгендерных женщин в сочетании с эстрогеном, обычно в дозе 50 мг/сут[16][55][56][57][58][59][60]
- Периферическое преждевременное половое созревание у мальчиков в дозе от 12,5 до 100 мг/сут в комбинации с ингибитором ароматазы, таким как анастрозол, особенно при наследственном преждевременном половом созревании, ограниченном у мужчин (тестотоксикоз)[24][61][62][63][64][65][17][66]
- Чрезмерно длительная эрекция у мужчин при приеме от 50 мг в неделю до 50 мг через день.[67][68][69][70][1][5][18]
Препарат был рекомендован для лечения, но его эффективность остается неопределенной при следующих показаниях:
- Гиперсексуальность и парафилии, особенно в сочетании с химической кастрацией[71][72][73][74][75][76]
Более подробную информацию об этих способах применения смотрите в статье "Применение бикалутамида в медицине".
Доступные формы[править | править код]
Бикалутамид доступен для лечения рака предстательной железы в большинстве развитых стран,[77][35][78] включая более 80 стран по всему миру.[36][37] Он выпускается в таблетках по 50 мг, 80 мг (в Японии)[45] и 150 мг для приема внутрь.[79][80] Препарат зарегистрирован для применения в качестве монотерапии в дозе 150 мг/сут для лечения местнораспространенного рака предстательной железы по меньшей мере в 55 странах. Заметным исключением является США, где он зарегистрирован только для применения в дозе 50 мг/сут в сочетании с кастрацией.[81] Никакие другие лекарственные формы или способы введения не доступны и не используются.[79] Все препараты бикалутамида специально предназначены для лечения рака предстательной железы отдельно или в сочетании с хирургической или медикаментозной кастрацией. Из-за низкой растворимости бикалутамида в воде, бикалутамид в таблетках для приема внутрь подвергается микронизации для обеспечения малого и однородного размера частиц и оптимизации биодоступности при приеме внутрь.[82]
Комбинированный препарат бикалутамида и агониста ГнРГ гозерелина, в который гозерелин вводится в виде подкожного имплантата для инъекций, а бикалутамид – в виде таблеток по 50 мг для приема внутрь, продается в Австралии и Новой Зеландии под торговой маркой ZolaCos CP (комбинированная упаковка Золадекса и Касодекса).[78][83][84][85]
Противопоказания[править | править код]
Бикалутамид относится к категории "беременность X", или "противопоказан при беременности", в США[24], а в Австралии - к категории "беременность D", которая является второй по значимости в списке запрещенных препаратов.[86]Таким образом, он противопоказан женщинам во время беременности, и женщинам, которые ведут активную половую жизнь и которые могут забеременеть, настоятельно рекомендуется принимать бикалутамид только в сочетании с адекватной контрацепцией.[87][88] Неизвестно, выделяется ли бикалутамид с грудным молоком, но многие лекарственные препараты выделяются с грудным молоком, и по этой причине лечение бикалутамидом также не рекомендуется во время грудного вскармливания.[1][24]
У лиц с тяжелой, но не легкой или умеренной печеночной недостаточностью имеются данные о том, что выведение бикалутамида замедляется, и, следовательно, у этих пациентов может быть необходима осторожность, поскольку уровень бикалутамида в крови может быть повышен.[89] При тяжелой печеночной недостаточности период полувыведения активного (R)-энантиомера бикалутамида увеличивается примерно в 1,75 раза (увеличение на 76%; период полувыведения составляет 5,9 и 10,4 дня у здоровых и ослабленных пациентов соответственно).[10][90][91] Период полувыведения бикалутамида при нарушении функции почек не изменяется.[81]
Побочные эффекты[править | править код]
Профиль побочных эффектов бикалутамида в значительной степени зависит от пола, то есть от того, является ли человек мужчиной или женщиной. У мужчин из-за недостатка андрогенов во время лечения бикалутамидом могут возникать различные побочные эффекты различной степени тяжести, наиболее распространенными из которых являются боль/болезненность в груди и гинекомастия (увеличение груди).[92][93] Гинекомастия встречается у 80% мужчин, получающих монотерапию бикалутамидом, и имеет легкую или умеренную степень тяжести более чем у 90% пострадавших мужчин.[93][94]В дополнение к изменениям груди, у мужчин может наблюдаться физическая феминизация и демаскулинизация в целом, включая снижение роста волос на теле, уменьшение мышечной массы и силы, женственные изменения в массе и распределении жира, уменьшение длины полового члена и объема спермы/эякулята.[92][95][19][96]Другие побочные эффекты, которые наблюдались у мужчин и которые аналогичным образом связаны с недостатком андрогенов, включают приливы жара, сексуальную дисфункцию (например, потерю либидо, эректильную дисфункцию), депрессию, усталость, слабость и анемию.[92][97][98] Однако у большинства мужчин при монотерапии бикалутамидом сохраняется сексуальная функция.[99][100] У женщин, из-за минимальной биологической значимости андрогенов для этого пола, [101][102] побочные эффекты чистых антиандрогенов или нестероидных антиандрогенов незначительны, и было обнаружено, что бикалутамид очень хорошо переносится.[22] Однако было обнаружено, что бикалутамид повышает уровень общего холестерина и холестерина ЛПНП у женщин.[103][104][54] Считается, что профиль немедикаментозных побочных эффектов бикалутамида (т.е. побочных эффектов, не связанных с его антиандрогенной активностью) аналогичен таковому при применении плацебо.[105] В любом случае, общие побочные эффекты бикалутамида, которые могут наблюдаться у представителей обоих полов, включают диарею, запор, боль в животе, тошноту, сухость кожи, зуд и сыпь.[97][1][106][107][108][109] Препарат хорошо переносится в более высоких дозах, чем 50 мг/сут, до 600 мг/сут, с редкими дополнительными побочными эффектами.[81][110][111]
Применение бикалутамида было связано с нарушениями функциональных показателей печени, такими как повышение уровня печеночных ферментов.[97][10] В рамках клинической программы лечения бикалутамидом раннего рака предстательной железы для локализованного рака предстательной железы и МРПЖ частота нарушений функциональных показателей печени при монотерапии бикалутамидом составила 3,4% по сравнению с 1,9% при применении плацебо.[10][112] Однако в других исследованиях были отмечены более высокие показатели, вплоть до 11%.[15][24] Изменения в печени, которые потребовали прекращения приема бикалутамида, такие как выраженное повышение активности печеночных ферментов или гепатит, в ходе клинических исследований наблюдались у 0,3-1,5% мужчин, или примерно у 1% в целом.[24][10][30][112][113] Повышение уровня печеночных ферментов при приеме бикалутамида обычно наблюдается в течение первых 3-6 месяцев лечения.[97][24]Во время лечения рекомендуется контролировать функцию печени, особенно в первые несколько месяцев.[10][92] Было обнаружено, что у мужчин с ранним раком предстательной железы монотерапия бикалутамидом увеличивает смертность от рака предстательной железы, не связанного с раком предстательной железы.[23][114][10] Причины увеличения смертности при применении бикалутамида у этих мужчин неизвестны, но возможные факторы могут включать дефицит андрогенов или токсичность бикалутамида, связанную с приемом лекарств.[115][116]
На сегодняшний день опубликовано 10 сообщений о случаях печеночной токсичности, связанной с бикалутамидом. 2022.[117][118][119][120] В 2 из этих случаев наступила смерть.[117][121][122] В базе данных Системы отчетности о нежелательных явлениях FDA (FAERS) имеются сотни дополнительных случаев осложнений со стороны печени у людей, принимающих бикалутамид.[123] Во всех опубликованных отчетах о случаях печеночной токсичности при применении бикалутамида симптомы появлялись в течение первых 6 месяцев лечения.[118][119][120] Симптомы, которые могут указывать на нарушение функции печени, включают тошноту, рвоту, боль в животе, усталость, анорексию, "гриппоподобные" симптомы, потемнение мочи и желтуху.[24] Также опубликованы сообщения о случаях интерстициального пневмонита и эозинофильных заболеваний легких, связанных с приемом бикалутамида.[124][125][126] наряду с сотнями дополнительных экземпляров в базе данных FAERS.[123] Интерстициальный пневмонит потенциально может прогрессировать до 0+ и привести к летальному исходу. Симптомы, которые могут указывать на дисфункцию легких, включают одышку (затрудненное дыхание), кашель и фарингит (воспаление глотки, приводящее к боли в горле).[127] Точная частота развития печеночной токсичности и интерстициального пневмонита при применении бикалутамида неизвестна, но считается, что и то, и другое встречается очень редко.[119][128][129] Сообщалось о нескольких случаях светочувствительности при применении бикалутамида.[25] Также редко сообщалось о реакциях гиперчувствительности (лекарственной аллергии), таких как ангионевротический отек и крапивница, связанных с приемом бикалутамида.[24]
Поскольку бикалутамид является антиандрогеном, теоретически существует риск врожденных дефектов, таких как атипичная вариативность половых органов у плодов мужского пола.[87][88][130][131] Из-за его тератогенной способности женщинам, принимающим бикалутамид, которые являются фертильными и сексуально активными, следует использовать контрацептивы.[132]
Сравнение[править | править код]
Профиль побочных эффектов бикалутамида у мужчин и женщин отличается от такового у других антиандрогенов и считается благоприятным по сравнению с ними.[133][100][134][135] По сравнению с аналогами ГнРГ и стероидным антиандрогеном ципротерон ацетатом (ЦПА) монотерапия бикалутамидом приводит к значительно меньшей частоте и тяжести приливов жара и сексуальной дисфункции.[99][100][94][136] Кроме того, в отличие от аналогов ГнРГ и ЦПА, монотерапия бикалутамидом не связана со снижением минеральной плотности костной ткани или остеопорозом.[94][100] И наоборот, монотерапия бикалутамидом связана с гораздо более высокими показателями болезненности молочных желез, гинекомастии и феминизации у мужчин, чем аналоги ГнРГ и ЦПА.[94]Однако гинекомастия при приеме бикалутамида редко бывает тяжелой, и частота отмены препарата из-за этого побочного эффекта довольно низкая.[94][100]Эти различия в побочных эффектах между монотерапией бикалутамидом, аналогами ГнРГ и ЦПА. объясняются тем фактом, что, в то время как аналоги ГнРГ и ЦПА. подавляют выработку эстрогена, монотерапия бикалутамидом не снижает уровень эстрогена, а фактически повышает его.[94]
Бикалутамид не связан с риском развития нервно-психических побочных эффектов, таких как утомляемость, а также сердечно-сосудистых побочных эффектов, таких как изменения свертываемости крови, образование тромбов, задержка жидкости, ишемическая кардиомиопатия и неблагоприятные изменения уровня липидов в сыворотке крови, с которыми был связан ЦПА.[136][137][138][139] У него гораздо более низкий риск гепатотоксичности, чем у флутамида и ЦПА, и интерстициального пневмонита, чем у нилутамида.[140][100][121][141][142][143] Препарат также не обладает такими уникальными рисками, как диарея при применении флутамида и тошнота, рвота, нарушения зрения и непереносимость алкоголя при применении нилутамида.[100][136][141] В отличие от энзалутамида, бикалутамид не вызывает судорог или связанных с ними центральных побочных эффектов, таких как беспокойство и бессонница.[144][145] Однако, хотя риск неблагоприятных изменений печени при применении бикалутамида невелик, энзалутамид отличается от бикалутамида отсутствием известного риска повышения активности печеночных ферментов или гепатотоксичности.[146][147] В отличие от спиронолактона, бикалутамид не оказывает антиминералокортикоидного действия[148] и, следовательно, не связан с гиперкалиемией, учащенным мочеиспусканием, дегидратацией, артериальной гипотензией или другими сопутствующими побочными эффектами.[149][150][151][136] У женщин, в отличие от ЦПА и спиронолактона, бикалутамид не вызывает нарушения менструального цикла или аменореи и не влияет на овуляцию или фертильность.[49][152]
Передозировка[править | править код]
Однократная пероральная доза бикалутамида у человека, которая вызывает симптомы передозировки или считается опасной для жизни, не установлена.[24][153] Дозы до 600 мг/сут хорошо переносились в клинических испытаниях[111]. Примечательно, что бикалутамид обеспечивает высокую степень всасывания, так что уровень его активного (R)-энантиомера в крови не повышается при дозировке выше 300 мг/сут.[111] Считается маловероятным, что передозировка бикалутамидом или другими НПВП первого поколения (например, флутамидом и нилутамидом) может представлять угрозу для жизни.[154] Массивная передозировка нилутамида (13 граммов, или в 43 раза превышающая нормальную максимальную клиническую дозу в 300 мг/сут) у 79-летнего мужчины прошла без осложнений, не вызвав никаких клинических признаков, симптомов или токсичности.[155] Специфического антидота при передозировке бикалутамидом или НПВП не существует, и лечение должно основываться на симптомах, если таковые имеются.[24][153]
Взаимодействия[править | править код]
Бикалутамид метаболизируется почти исключительно CYP3A4.Таким образом, его уровень в организме может изменяться ингибиторами и индукторами CYP3A4.[5](Список ингибиторов и индукторов CYP3A4 приведен здесь.) Однако, несмотря на то, что бикалутамид метаболизируется CYP3A4, нет данных о клинически значимых лекарственных взаимодействиях при одновременном применении бикалутамида в дозе 150 мг/сут или менее с препаратами, которые ингибируют или индуцируют активность фермента цитохрома Р450.[10]
Исследования In vitro показывают, что бикалутамид может быть способен ингибировать CYP3A4 и, в меньшей степени, CYP2C9, CYP2C19 и CYP2D6.И наоборот, исследования на животных показывают, что бикалутамид может индуцировать ферменты цитохрома Р450.В ходе клинического исследования одновременное применение бикалутамида с субстратом CYP3A4 мидазоламом вызывало лишь небольшое и статистически незначимое повышение уровня мидазолама (+27%), предположительно, вследствие ингибирования CYP3A4. Однако это было значительно ниже увеличения экспозиции мидазолама при применении таких мощных ингибиторов CYP3A4, как кетоконазол (+1500%), итраконазол (+1000%) и эритромицин (+350%), и считается, что это не имеет клинического значения. Нет никаких признаков клинически значимого ингибирования или индукции ферментов при применении бикалутамида в дозах 150 мг/сут или ниже.
Поскольку бикалутамид циркулирует в относительно высоких концентрациях и хорошо связывается с белками плазмы, он потенциально может вытеснить другие препараты, которые хорошо связываются с белками плазмы, такие как варфарин, фенитоин, теофиллин и аспирин.[93][97] Это, в свою очередь, может привести к увеличению свободных концентраций таких лекарственных средств и усилению их действия и/или побочных эффектов, что может потребовать коррекции дозы.[93] Было установлено, что бикалутамид, в частности, вытесняет кумариновые антикоагулянты, такие как варфарин, из связывающих их белков плазмы (а именно альбумина) in vitro, что потенциально приводит к усилению антикоагулянтного эффекта, и по этой причине при применении бикалутамида в комбинации с этими препаратами рекомендуется тщательный мониторинг протромбинового времени и при необходимости коррекция дозы.[156][157][158] Однако, несмотря на это, в ходе клинических испытаний, в которых приняли участие почти 3000 пациентов, не было обнаружено убедительных доказательств взаимодействия бикалутамида с другими лекарственными средствами.[97]
Фармакология[править | править код]
Антиандрогенная активность[править | править код]
Бикалутамид действует как высокоселективный конкурентный тихий антагонист андрогенных рецепторов (IC50 Tooltip = 159-243 нМ), основной биологической мишени андрогенных половых гормонов тестостерона и дигидротестостерона, и, следовательно, является антиандрогеном.[27][159][160][161] Активность бикалутамида заключается в (R)-изомере.[162] Благодаря своей селективности в отношении AR бикалутамид практически не взаимодействует с рецепторами других стероидных гормонов и, следовательно, не обладает клинически значимой гормональной активностью (например, прогестагенной, эстрогенной, глюкокортикоидной, антиминералокортикоидной).[163][31][164][42] Однако сообщалось, что бикалутамид обладает слабым сродством к рецептору прогестерона, антагонистом которого он является, и, следовательно, может обладать некоторой антипрогестагенной активностью.[165]Бикалутамид не ингибирует 5α-редуктазу и, как известно, не ингибирует другие ферменты, участвующие в стероидогенезе андрогенов (например, CYP17A1).[166]Хотя бикалутамид не связывается с рецепторами эстрогена (ERS), он может повышать уровень эстрогена вторично по отношению к блокаде андрогенных рецепторов при использовании в качестве монотерапии у мужчин и, следовательно, может оказывать некоторые косвенные эстрогенные эффекты у мужчин.[167] Бикалутамид не подавляет и не ингибирует выработку андрогенов в организме (т.е. он не действует как антигонадотропин или ингибитор стероидогенеза андрогенов или не снижает уровень андрогенов) и, следовательно, исключительно опосредует свои антиандрогенные эффекты, противодействуя андрогенным рецептарам.[1][163][162] В дополнение к классическому ядерным рецепторам, бикалутамид был исследован на мембранных андрогенных рецепторах и показал, что он действует как мощный антагонист ZIP9 ([[IC50|IC50]] = 66,3 нМ), в то время как с GPRC6A он, по-видимому, не взаимодействует.[168][169]
Сродство бикалутамида к андрогенным рецепторам относительно низкое, поскольку оно примерно в 30-100 раз ниже, чем у дигидротестостерона, который в 2,5-10 раз эффективнее агониста андрогенных рецепторов , чем тестостерон в биоанализах, и является основным эндогенным лигандом рецептора в предстательной железе.[170][161][171] Однако типичные клинические дозы бикалутамида приводят к тому, что уровни препарата в крови в тысячи раз превышают уровни тестостерона и дигидротестостерона, что позволяет ему эффективно предотвращать их связывание с рецепторами и активацию.[172][173][31][174][24][86][175][10][176] Это особенно верно в случае хирургической или медикаментозной кастрации, при которой уровень тестостерона в крови снижается примерно на 95%, а уровень ДГТ в предстательной железе - примерно на 50-60%.[161][177] У женщин уровень тестостерона значительно ниже (в 20-40 раз), чем у мужчин[178], поэтому необходимы гораздо меньшие дозы бикалутамида (например, 25 мг/сут в исследованиях гирсутизма).[14][49][179][30]
Блокада бикалутамидом андрогенных рецепторов в гипофизе и гипоталамусе приводит к предотвращению негативной обратной связи андрогенов с гипоталамо–гипофизарно–гонадной системой у мужчин и, как следствие, к растормаживанию секреции гипофизом лютеинизирующего гормона (ЛГ).[99] Это, в свою очередь, приводит к повышению уровня циркулирующего лютенинизирующего гормона и активации выработки тестостерона половыми железами и, как следствие, эстрадиола.[180] Было обнаружено, что уровень тестостерона повышается в 1,5-2 раза (на 59-97%), а уровень эстрадиола - примерно в 1,5-2,5 раза (на 65-146%) у мужчин, получавших монотерапию бикалутамидом в дозе 150 мг/сут.[28][29][30] В дополнение к тестостерону и эстрадиолу наблюдается небольшое повышение концентрации дигидротестостерона, глобулина, связывающего половые гормоны, и пролактина.[30] Уровни эстрадиола при монотерапии бикалутамидом аналогичны таковым у женщин в пременопаузе, в то время как уровень тестостерона, как правило, остается на высоком уровне у мужчин.[29][181][163] Концентрация тестостерона обычно не превышает нормальную для мужчин норму из-за отрицательной обратной связи на гипоталамо–гипофизарно-гонадной оси из-за повышенной концентрации эстрадиола.[99] Бикалутамид влияет на ось гипоталамо–гипофизарно-гонадную ось и повышает уровень гормонов только у мужчин, но не у женщин.[182][183][184] Это связано с гораздо более низким уровнем андрогенов у женщин и отсутствием у них базального подавления гипоталамо–гипофизарно-гонадной оси у представителей этого пола.[182][183][184] Как свидетельствует его эффективность при лечении рака предстательной железы и других андрогензависимых состояний, антиандрогенное действие бикалутамида значительно превосходит любое воздействие повышенного уровня тестостерона, к которому он приводит.[81] Однако бикалутамид не оказывает противодействия повышенному уровню эстрадиола и является причиной гинекомастии и феминизирующих побочных эффектов, которые он вызывает у мужчин.[185]Хотя монотерапия бикалутамидом повышает уровень гонадотропинов и половых гормонов у мужчин, этого не произойдет, если бикалутамид сочетать с антигонадотропинами, такими как аналоги ГнРГ, эстрогены или прогестагены, поскольку эти препараты поддерживают отрицательную обратную связь по оси HPG.[47][186][187]
При нормальных обстоятельствах бикалутамид не способен активировать андрогенные рецепторы.[188][189] Однако при раке предстательной железы мутации и избыточная экспрессия андрогенных рецепторов могут накапливаться в клетках предстательной железы, которые могут превращать бикалутамид из антагониста андрогенных рецепторов в агонист.[188][190] Это может привести к парадоксальной стимуляции роста рака предстательной железы бикалутамидом и является причиной синдрома отмены антиандрогенов, при котором прекращение приема антиандрогенов парадоксальным образом замедляет темпы роста рака предстательной железы.[188][190]
У трансгендерных женщин развитие груди является желательным эффектом лечения антиандрогенами или эстрогенами.[60][191] Считается, что развитие молочных желез и гинекомастия, вызванные бикалутамидом, опосредуются повышенной активацией эстрогенного рецептора, вторичной по отношению к блокаде андрогенных рецепторов (что приводит к растормаживанию эстрогенного рецептора в тканях молочной железы) и повышению уровня эстрадиола.[17][192][193] Было обнаружено, что бикалутамид, помимо отложения жира, роста соединительной ткани и развития протоков, способствует умеренному дольково-альвеолярному развитию молочных желез.[194][195][196] Однако полное созревание дольково-альвеолярного отростка, необходимое для лактации и грудного вскармливания, не произойдет без лечения прогестагенами.[194][195][196]
Монотерапия бикалутамидом, по-видимому, оказывает минимальное влияние на сперматогенез яичек, ультраструктуру яичек и некоторые аспекты мужской фертильности.[197][87][198] По-видимому, это связано с тем, что уровень тестостерона в яичках (где вырабатывается ~95% тестостерона у мужчин) чрезвычайно высок (до 200 раз превышает уровень в крови), и только небольшая часть (менее 10%) от нормального уровня тестостерона в яичках на самом деле необходима для поддержания нормального уровня тестостерона в яичках. поддерживайте сперматогенез.[199][200][201] В результате бикалутамид, по-видимому, не в состоянии конкурировать с тестостероном в этой единственной части тела в степени, достаточной для существенного нарушения передачи сигналов и функционирования андрогенов.[199][200][201] Однако, хотя бикалутамид, по-видимому, не способен отрицательно влиять на сперматогенез яичек, он может препятствовать созреванию сперматозоидов, зависящему от АР, и их транспортировке за пределы яичек в придатки и семявыводящий проток, где уровень андрогенов намного ниже, и, следовательно, все еще может снижать мужскую фертильность.[202]Кроме того, комбинация бикалутамида с другими лекарственными препаратами, такими как эстрогены, прогестагены и аналоги ГнРГ, может нарушать сперматогенез из-за их собственного неблагоприятного воздействия на мужскую фертильность.[203][204][205][206][207][208] Эти препараты способны сильно подавлять выработку андрогенов гонадами, что может серьезно ухудшить или вовсе отменить сперматогенез в яичках, и эстрогены, по-видимому, также оказывают прямое и потенциально длительное цитотоксическое действие на яички в достаточно высоких концентрациях.[203][204][205][206][207][208]
Другая[править | править код]
В ходе доклинических исследований было обнаружено, что бикалутамид действует как ингибитор или индуктор некоторых ферментов цитохрома Р450, включая CYP3A4, CYP2C9, CYP2C19 и CYP2D6, но никаких доказательств этого у людей, получавших препарат в дозе до 150 мг/сут, обнаружено не было.Он также был идентифицирован in vitro как сильный ингибитор CYP27A1 (холестерин-27-гидроксилазы) и CYP46A1 (холестерин-24-гидроксилазы), но это еще предстоит оценить или подтвердить in vivo или у людей, и клиническое значение остается неизвестным.[209][210] Было обнаружено, что бикалутамид является ингибитором Р-гликопротеина (ABCB1).[211][212][213] Как и другие НПВП первого поколения и энзалутамид, он, как было обнаружено, действует как слабый неконкурентный ингибитор токов, опосредованных ГАМК-рецепторами, in vitro ([[IC50|IC50]] = 5,2 мкм).[214][215]Однако, в отличие от энзалутамида, не было обнаружено связи бикалутамида с судорогами или другими сопутствующими побочными эффектами со стороны центральной нервной системы, поэтому клиническая значимость этого открытия остается неопределенной.[214][215]
Хотя его абсолютная биодоступность для человека неизвестна, известно, что бикалутамид интенсивно и хорошо всасывается.[1] Пища не влияет на его усвоение.[1][156] Всасывание бикалутамида является линейным при дозах до 150 мг/сут и является насыщающим при дозах выше этого уровня, при этом при дозах выше 300 мг/сут дальнейшего повышения равновесных уровней бикалутамида не происходит.[10][216][111] В то время как всасывание (R)-бикалутамида происходит медленно, его концентрация достигает максимума через 31-39 часов после приема, (S)-бикалутамид всасывается гораздо быстрее.[10][24] Стабильные концентрации препарата достигаются через 4-12 недель лечения независимо от дозы, при этом уровень (R)-бикалутамида постепенно повышается в 10-20 раз.[10][217][218][175] Длительное достижение стабильных уровней является результатом очень длительного периода полувыведения бикалутамида.[175] Уровни (R)-бикалутамида варьируют между людьми в широких пределах (до 16 раз) при применении бикалутамида независимо от дозы.
Распределение бикалутамида в тканях точно не изучено[219].Количество бикалутамида в сперме, которое потенциально может передаваться партнерше во время полового акта, невелико и не считается важным.[86] На основании исследований на животных с участием крыс и собак предполагалось, что бикалутамид не может проникать через гематоэнцефалический барьер и, следовательно, не может проникать в мозг.[220][31][221][222] Как таковой, первоначально считалось, что это периферийно-селективный антиандроген.[220][31] Однако последующие клинические исследования показали, что это не относится к людям, что указывает на видовые различия; бикалутамид проникает в мозг человека и, соответственно, вызывает эффекты и побочные эффекты, соответствующие центральному антиандрогенному действию.[99][223][224][225] В любом случае, есть признаки того, что бикалутамид может обладать, по крайней мере, некоторой периферической селективностью у людей.[226] Бикалутамид хорошо связывается с белками плазмы (96,1% для рацемического бикалутамида, 99,6% для (R)-бикалутамида) и связывается в основном с альбумином, при незначительном связывании с глобулином, связывающим половые гормоны и глобулином, связывающим кортикостероиды.[219][166]
Бикалутамид метаболизируется в печени.[156] (R)-бикалутамид метаболизируется медленно и почти исключительно путем гидроксилирования CYP3A4 в (R)-гидроксибикалутамид.[156][227] Затем этот метаболит глюкуронируется UGT1A9.[156][4] В отличие от (R)-бикалутамида, (S)-бикалутамид метаболизируется быстро и в основном путем глюкуронирования (без гидроксилирования).[156] Известно, что ни один из метаболитов бикалутамида не является активным, и уровни метаболитов в плазме крови, где преобладает неизмененный биклаутамид, низкие. Из-за стереоселективного метаболизма бикалутамида, (R)-бикалутамид имеет гораздо более длительный конечный период полувыведения, чем (S)-бикалутамид, и его уровни примерно в 10-20 раз выше по сравнению с однократным приемом и в 100 раз выше в равновесном состоянии.[10][227][228](R) - Бикалутамид имеет относительно длительный период полувыведения - 5,8 дней при однократном приеме и 7-10 дней после повторного приема.[6]
Бикалутамид выводится в одинаковых пропорциях с калом (43%) и мочой (34%), в то время как его метаболиты выводятся примерно поровну с мочой и желчью.[156][229][230] Препарат выводится из организма в значительной степени в неметаболизированном виде, и как бикалутамид, так и его метаболиты выводятся в основном в виде глюкуронидных конъюгатов.[162] Глюкуронидные конъюгаты бикалутамида и его метаболиты быстро выводятся из организма, в отличие от неконъюгированного бикалутамида.[156][231]
На фармакокинетику бикалутамида не влияют потребление пищи, возраст или масса тела человека, нарушение функции почек или печени легкой и умеренной степени тяжести.[175]Однако устойчивые уровни бикалутамида у японцев выше, чем у белых людей.Шаблон:Bicalutamide metabolism
Химия[править | править код]
Бикалутамид представляет собой рацемическую смесь, состоящую из равных пропорций энантиомеров (R)-бикалутамида (правовращающего) и (S)-бикалутамида (левовращающего).[24] Его систематическое название таково (RS)-N-[4-cyano-3-(trifluoromethyl)phenyl]-3-[(4-fluorophenyl)sulfonyl]-2-hydroxy-2-methylpropanamide.[232][233] Соединение имеет химическую формулу C18h14f4n2o4s, молекулярную массу 430,373 г/моль и представляет собой мелкий порошок от белого до темно-белого цвета.[1][4[86]
Константа кислотной диссоциации (pKa') бикалутамида составляет приблизительно 12.[86] Это высоколипофильное соединение (log P = 2.92).[234] При температуре 37 °C (98,6 °F), или нормальной температуре тела человека, бикалутамид практически не растворим в воде (4,6 мг/л), кислоте (4,6 мг/л при рН 1) и щелочи (3,7 мг/л при рН 8).[24][86]В органических растворителях он слабо растворим в хлороформе и абсолютном этаноле, слабо растворим в метаноле и свободно растворим в ацетоне и тетрагидрофуране.[24][86]
Бикалутамид - это синтетическое нестероидное соединение, полученное из флутамида.[235] Это бициклическое соединение (имеет два кольца), которое может быть классифицировано как анилид (N-фениламид) или анилин, диарилпропионамид и толуидид.[235][227]
Аналоги[править | править код]
НПВП первого поколения, включая бикалутамид, флутамид и нилутамид, являются синтетическими нестероидными производными анилидов и структурными аналогами друг друга.[235] Бикалутамид - это диарилпропионамид, в то время как флутамид - моноарилпропионамид, а нилутамид - гидантоин.[235] Бикалутамид и флутамид, хотя и не нилутамид, также могут быть отнесены к толуидидам.[227] Все три соединения имеют общую 3-трифторметиланилиновую часть.[236] Бикалутамид - это модификация флутамида, в которую был добавлен 4-фторфенилсульфонильный фрагмент, а нитрогруппа в исходном фенильном кольце была заменена цианогруппой.[237]Топилутамид, также известный как флуридил, является еще НПВП, который структурно близок к НПВП первого поколения, но, в отличие от них, не используется при лечении рака предстательной железы, а вместо этого используется исключительно в качестве местного антиандрогена при лечении типичного выпадения волос.[238][239][240]
НПВП второго поколения энзалутамид и апалутамид были получены из НПВП первого поколения являются их аналогами[156][241], в то время как другой НПВП второго поколения, даролутамид, как утверждается, структурно отличается и химически не связан с другими.[242] Энзалутамид представляет собой модификацию бикалутамида, в которой межкольцевая связующая цепь была изменена и циклизована в 5,5-диметил-4-оксо-2-тиоксо имидазолидиновый фрагмент. В апалутамиде 5,5-диметильные группы имидазолидинового кольца энзалутамида циклизуются с образованием дополнительного циклобутанового кольца, а одно из его фенильных колец заменяется пиридиновым кольцом.Шаблон:Annotated image 4Первые нестероидные андрогены, арилпропионамиды, были открыты с помощью структурной модификации бикалутамида.[243] В отличие от бикалутамида (который обладает чисто антиандрогенным действием), эти соединения проявляют тканеселективные андрогенные эффекты и были классифицированы как селективные модуляторы андрогенных рецепторов[243], препараты этой серии включали ацетотиолутамид, энобосарм (остарин; S-22) и андарин (ацетамидоксолутамид или андроксолутамид; S-4).[235][243][244] Они очень близки к бикалутамиду по структуре, с ключевыми отличиями, заключающимися в том, что связующий сульфон бикалутамида был заменен простой или тиоэфирной группой для придания агонизирующего действия AR, а 4-фтористый атом соответствующего фенильного кольца был заменен ацетамидо- или цианогруппой для устранения реакционной способности в этом положении..[245]
Было разработано несколько радиоактивно меченых производных бикалутамида для потенциального использования в качестве радиоактивных индикаторов в медицинской визуализации.[246][247] К ним относятся [18%] бикалутамид, 4- [76%]бромобикалутамид и [76%]бромотиобикалутамид.[246][247] Было обнаружено, что последние два препарата обладают значительно повышенным сродством к андрогенным рецепторам по сравнению с бикаутамидом.[246] Однако ни один из этих препаратов не был испытан на людях.[246][247]
5n-бикалутамид, или 5-азабикалутамид, представляет собой незначительную структурную модификацию бикалутамида, который действует как обратимый ковалентный антагонист андрогенных рецепторов и обладает примерно в 150 раз более высоким сродством к андрогенным рецепторам и примерно в 20 раз большим функциональным ингибированием андрогенных рецепторов по сравнению с бикалутамидом.[248][249] Он является одним из наиболее мощных антагонистов андрогенных рецепторов, которые были разработаны, и в настоящее время изучается для потенциального использования в лечении антиандрогенрезистентного рака предстательной железы.[248]
Синтез[править | править код]
В литературе опубликован ряд результатов химического синтеза бикалутамида.[232][250][251][252] Процедуру первого опубликованного синтеза бикалутамида можно увидеть ниже.[250]
История[править | править код]
Бикалутамид, как и все другие НПВП, представленные на рынке нестероидные антиандрогены настоящее время, были получены путем структурной модификации флутамида, который сам по себе был первоначально синтезирован в качестве бактериостатического средства в 1967 году корпорацией Schering Plough Corporation и, как впоследствии было установлено, обладает антиандрогенной активностью.[253][254][255] Бикалутамид был открыт Такером и его коллегами из Imperial Chemical Industries (ICI) в 1980-х годах и был выбран для разработки из более чем 2000 синтезированных соединений.[256][166][257][232] Впервые он был запатентован в 1982 году[258] и впервые опубликован в научной литературе в июне 1987 года[259]
Бикалутамид был впервые изучен в ходе клинического клинического исследования 1987 году[97], а результаты первого клинического исследования II фазы при раке предстательной железы были опубликованы в 1990 году[260].Фармацевтическое подразделение ICI было выделено в независимую компанию Zeneca в 1993 году, а в апреле и мае 1995 года Zeneca (ныне AstraZeneca, после слияния с Astra AB в 1999 году) начала предварительную продажу бикалутамида для лечения рака предстательной железы в США[261]Впервые он был представлен в Великобритании в мае 1995 года[262] и впоследствии был одобрен Управлением по санитарному надзору за качеством пищевых продуктов и FDA 4 октября 1995 года для лечения рака предстательной железы в дозе 50 мг/сут в сочетании с аналогом ГнРГ.[263][264]
После введения бикалутамида для применения в комбинации с аналогом гонадотропин-рилизинг-гормона бикалутамид был разработан в качестве монотерапии в дозировке 150 мг/сут для лечения рака предстательной железы и был одобрен по этому показанию в Европе, Канаде и ряде других стран в конце 1990-х и начале 2000-х годов.[10][161][265][266] Это применение бикалутамида также рассматривалось Управлением по санитарному надзору за качеством пищевых продуктов и FDA в 2002 году[267], но в конечном итоге не было одобрено в этой стране.[81] В Японии бикалутамид разрешен к применению в дозировке 80 мг/сут отдельно или в комбинации с аналогом гонадотропин-рилизинг-гормона для лечения рака предстательной железы.[45] Уникальная дозировка бикалутамида в 80 мг, используемая в Японии, была выбрана для разработки в этой стране на основе наблюдаемых фармакокинетических различий с бикалутамидом у японских мужчин.[46]
После получения отрицательных результатов монотерапии бикалутамидом при локализованного рака предстательной железы в рамках клинической программы раннего рака предстательной железы, разрешение на использование бикалутамида специально для лечения локализованного рак предстательной железы было отозвано в ряде стран[11], включая Великобританию (в октябре или ноябре 2003 г.)[12] и несколько других европейских стран и Канаду (в августе 2003 г.).[10][268][269] Кроме того, в США и Канаде по этим показаниям категорически не рекомендуется принимать бикалутамид в дозе 150 мг/сут.[13] С другой стороны, препарат эффективен для лечения локализованного рака предстательной железы и метастатического рака предстательной железы, остается одобренным и продолжает использоваться при лечении местнораспространенного рака предстательной железы и метастатического рака предстательной железы.[10]
Срок действия патента на бикалутамид в США истек в марте 2009 года, и впоследствии препарат был доступен в качестве дженерика[270] по значительно сниженной цене.[271]
Бикалутамид стал четвертым антиандрогеном (и третьим нестероидным антиандрогеном), который был введен для лечения рака предстательной железы, после стероидного антиандрогена ципротерона ацетата в 1973 году[272] и флутамида НПВП в 1983 году (1989 год в США)[232][273] и нилутамида в 1989 году (1996 год в США).[236][274][275] За ним последовали абиратерона ацетат в 2011 году, энзалутамид в 2012 году, апалутамид в 2018 году и даролутамид в 2019 году, а также, возможно, такие разрабатываемые препараты, как проксалутамид и севитеронел.[276]
Общество и культура[править | править код]
Общие названия[править | править код]
Бикалутамид - это общее название лекарственного средства на английском и французском языках, а так же его международное непатентованное название. [35][277][77][278] Он также упоминается как бикалутамид на латыни, бикалутамида на испанском и португальском языках, бикалутамид на немецком и бикалутамид на русском и других славянских языках.[35][77] Префикс "bica-" соответствует тому факту, что бикалутамид является бициклическим соединением, в то время как суффикс "-лютамид" является стандартным суффиксом для нестероидных антиандрогенов.[279][280] Бикалутамид также известен под своим прежним кодовым названием ICI-176,334.[277][77][35]
Фирменные наименования[править | править код]
Бикалутамид продается компанией AstraZeneca в форме таблеток для приема внутрь под торговыми марками Касодекс, Косудекс, Калутид, Калумид и Калумид во многих странах.[35][77][281][282] В различных странах он также продается под торговыми марками Бикадекс, Бикал, Бикалокс, Бикамид, Бикатлон, Бикузан, Бинабик, Байпро, Калутол и Ормандил, а также под другими.[35] Препарат продается под большим количеством непатентованных торговых названий, таких как Апо-бикалутамид, Бикалутамид Аккорд, бикалутамид Актавис, Бикалутамид Блюфиш, Бикалутамид Каби, Бикалутамид Сандоз и бикалутамид Тева.[35] Комбинированный препарат бикалутамида и гозерелина продается компанией AstraZeneca в Австралии и Новой Зеландии под торговой маркой ZolaCos-CP.[78][83][84][85]
Стоимость и дженерики[править | править код]
Бикалутамид не запатентован и доступен в виде дженерика.[270]В отличие от бикалутамида, новый нестероидный антиандроген энзалутамид все еще находится в стадии патентования и по этой причине значительно дороже по сравнению с ним.[283]
Срок действия патентов на все три НПВП первого поколения истек, и флутамид и бикалутамид доступны в качестве недорогих дженериков.[284][285] Нилутамид, с другой стороны, всегда был слабым третьим конкурентом флутамиду и бикалутамиду и, в связи с этим, не был разработан как дженерик и доступен только под торговой маркой Nilandron, по крайней мере, в США[284][285]
Бикалутамид значительно дешевле аналогов ГнРГ, которые, несмотря на то, что на некоторые из них уже много лет нет патента, как сообщалось (в 2013 году), обычно обходятся в 10 000-15 $10,000 США в год (или около $1,000 США в месяц) на лечение.[286][287]
Продажи бикалутамида (также известного как Казодекс) по всему миру достигли пика в 1,3 миллиарда долларов в 2007 году[288], и его называли препаратом стоимостью "миллиард долларов в год" до того, как он потерял свою патентную защиту, начиная с 2007 года. 2007.[40][289][238] В 2014 году, несмотря на введение абиратерона ацетата в 2011 году и энзалутамида в 2012 году, бикалутамид по-прежнему оставался наиболее часто назначаемым препаратом для лечения метастатического кастрационно-резистентного рака предстательной железы.[40]Более того, несмотря на то, что бикалутамид не был запатентован, продажи AstraZeneca по-прежнему приносили несколько сотен миллионов долларов в год.[40] Общий объем мировых продаж торговой марки Casodex на конец года составил около 13,4миллиарда . 2018.[290][291][37][292][293][288][294][295][296][297][298] [чрезмерное количество цитат]
| Год | Продажи | Год | Продажи | Год | Продажи | Год | Продажи | Год | Продажи | Год | Продажи | Год | Продажи | Год | Продажи |
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 1995 | ~15 миллионов долларов | 1998 | 245 миллионов долларов | 2001 | $569 млн | 2004 | $1012 млн | 2007* | $1335 млн | 2010 | $579 млн | 2013 | $376 млн | 2016 | 247 миллионов долларов |
| 1996 | 109 миллионов долларов | 1999 | 340 миллионов долларов | 2002 | $644 млн | 2005 | $1123 млн | 2008 | $1258 млн | 2011 | 550 миллионов долларов | 2014 | 320 миллионов долларов | 2017 | 215 миллионов долларов |
| 1997 | 200 миллионов долларов | 2000 | $433 млн | 2003 | $854 млн | 2006 | $1206 млн | 2009 | $844 млн | 2012 | $454 млн | 2015 | 267 миллионов долларов | 2018 | $201 млн |
| Примечания: Впервые дженерик появился в продаже (*) в 2007 году.[289]Общий объем продаж по состоянию на конец 2018 года составил 13,4 миллиарда долларов. Источники:[290][291][37][292][293][288][294][295][296][297][298] | |||||||||||||||
В период с января 2007 по декабрь 2009 года (в течение трех лет) в США было выписано 1 232 143 рецепта на бикалутамид, или около 400 000 рецептов в год.[41] За это время на бикалутамид приходилось около 87,2% рынка НПВП, на флутамид - 10,5%, а на нилутамид - 2,3%.[41] Примерно 96% рецептов на бикалутамид были выписаны с использованием диагностических кодов, которые четко указывали на новообразование.[41]Около 1200 рецептов на бикалутамид, или 0,1% от общего числа, были выписаны детям в возрасте от 0 до 16 лет[41]
Регулирование[править | править код]
Бикалутамид отпускается по рецепту врача.[80] Ни в одной стране это вещество специально не контролируется и, следовательно, не является запрещенным веществом.[7] Однако производство, продажа, дистрибуция и хранение отпускаемых по рецепту лекарств по-прежнему являются предметом правового регулирования во всем мире.[299][300][301]
Исследование[править | править код]
Бикалутамид был изучен в комбинации с ингибиторами 5α-редуктазы финастеридом и дутастеридом при раке предстательной железы.[302][303][304][305][306][307][308] Он также был изучен в комбинации с ралоксифеном, селективным модулятором рецепторов эстрогена (SERM), для лечения рака предстательной железы.[309][310] Бикалутамид был протестирован для лечения АР-положительного, эстроген-и-прогестеронновых-рецептеров-отрицательного местнораспространенного и метастатического рака молочной железы у женщин в ходе исследования II фазы по этим показаниям.[311][312][313] Энзалутамид также исследуется при лечении этого типа рака.[314][315] Бикалутамид также был изучен в ходе II фазы клинических испытаний по лечению рака яичников у женщин[316]
Бикалутамид был изучен при лечении доброкачественной гиперплазии предстательной железы (ДГПЖ) в ходе 24-недельного исследования с участием 15 пациентов в дозе 50 мг/сут.[317][318]У пациентов, принимавших бикалутамид, объем предстательной железы уменьшился на 26%, а показатели симптомов раздражения мочевыводящих путей значительно снизились.[317][318] И наоборот, показатели пиковой скорости мочеиспускания и давления мочи существенно не отличались между бикалутамидом и плацебо.[317][318]Уменьшение объема предстательной железы, достигнутое при применении бикалутамида, было сопоставимо с таковым при применении ингибитора 5α-редуктазы финастерида, который одобрен для лечения аденомы простаты.[319][320]Болезненность молочных желез (93%), гинекомастия (54%) и сексуальная дисфункция (60%) были зарегистрированы как побочные эффекты бикалутамида в дозировке, использованной в исследовании, хотя прекращения лечения из-за побочных эффектов не произошло, и сексуальная активность была сохранена у 75% пациенток.[318][97]
В 2017 году в Италии под наблюдением Итальянского агентства по лекарственным средствам (AIFA) было завершено клиническое исследование III фазы бикалутамида в комбинации с содержащим этинилэстрадиол для лечения тяжелого гирсутизма у женщин с СПКЯ.[54]
Для лечения COVID-19 у мужчин были предложены антиандрогены, и по состоянию на май 2020 года для этой цели проводится вторая фаза клинических испытаний бикалутамида в высоких дозах.[321][322]
Использование в ветеринарии[править | править код]
Бикалутамид может быть использован для лечения гиперандрогении и связанной с ней доброкачественной гиперплазии предстательной железы, вторичной по отношению к гиперадренокортицизму (вызванному избытком андрогенов надпочечников) у самцов хорьков.[323][324][325] Однако он не был официально оценен в контролируемых исследованиях с этой целью.[325][326]
- Сравнение бикалутамида с другими антиандрогенами
Примечания[править | править код]
- ↑ 1 2 3 4 5 6 7 8 9 10 Medical Toxicology. — Lippincott Williams & Wilkins, 2004. — P. 497, 521. — ISBN 978-0-7817-2845-4.
- ↑ 1 2 3 Ошибка в сносках?: Неверный тег
<ref>; для сносокCockshott2004не указан текст - ↑ 1 2 3 Foye's Principles of Medicinal Chemistry. — Lippincott Williams & Wilkins, 2008. — P. 121, 1288, 1290. — ISBN 978-0-7817-6879-5.
- ↑ 1 2 Grosse L, Campeau AS, Caron S, Morin FA, Meunier K, Trottier J, Caron P, Verreault M, Barbier O (August 2013). "Enantiomer selective glucuronidation of the non-steroidal pure anti-androgen bicalutamide by human liver and kidney: role of the human UDP-glucuronosyltransferase (UGT)1A9 enzyme". Basic & Clinical Pharmacology & Toxicology. 113 (2): 92—102. doi:10.1111/bcpt.12071. PMC 3815647. PMID 23527766.
- ↑ 1 2 3 Mosby's 2014 Nursing Drug Reference – Elsevieron VitalSource. — Elsevier Health Sciences, 17 April 2013. — P. 193–194. — ISBN 978-0-323-22267-9.
- ↑ 1 2 Hormone Therapy in Breast and Prostate Cancer. — Springer Science & Business Media, 5 February 2010. — P. 350–. — ISBN 978-1-59259-152-7.
- ↑ 1 2 3 4 5 6 7 8 9 10 Bicalutamide. The American Society of Health-System Pharmacists. Дата обращения: 8 декабря 2016. Архивировано 29 декабря 2016 года.
- ↑ Oxford Textbook of Endocrinology and Diabetes. — OUP Oxford, 28 July 2011. — P. 1625–. — ISBN 978-0-19-923529-2.
- ↑ Medical Therapy in Urology : [англ.]. — Springer Science & Business Media, 2010. — P. 40. — ISBN 9781848827042.
- ↑ 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 Wellington K, Keam SJ (2006). "Bicalutamide 150mg: a review of its use in the treatment of locally advanced prostate cancer" (PDF). Drugs. 66 (6): 837—50. doi:10.2165/00003495-200666060-00007. PMID 16706554. S2CID 46966712. Архивировано из оригинала (PDF) 28 августа 2016. Дата обращения: 13 августа 2016.
- ↑ 1 2 Shahani R, Fleshner NE, Zlotta AR (2007). "Pharmacotherapy for prostate cancer: the role of hormonal treatment". Discovery Medicine. 7 (39): 118—24. PMID 18093474. Архивировано 9 августа 2020. Дата обращения: 13 августа 2016.
- ↑ 1 2 Challenges in Prostate Cancer. — John Wiley & Sons, 15 April 2008. — P. 146–. — ISBN 978-1-4051-7177-9.
- ↑ 1 2 Urological Oncology. — Springer, 17 January 2015. — P. 823–. — «On the other hand, the 150 mg dose of bicalutamide has been associated with some safety concerns, such as a higher death rate when added to active surveillance in the early prostate cancer trialists group study [29], which has led the United States and Canada to recommend against prescribing the 150 mg dose [30].». — ISBN 978-0-85729-482-1.
- ↑ 1 2 3 Evidence-Based Dermatology. — John Wiley & Sons, 22 January 2009. — P. 529–. — ISBN 978-1-4443-0017-8.
- ↑ 1 2 Carvalho RM, Santos LD, Ramos PM, Machado CJ, Acioly P, Frattini SC, Barcaui CB, Donda AL, Melo DF (January 2022). "Bicalutamide and the new perspectives for female pattern hair loss treatment: What dermatologists should know". J Cosmet Dermatol. 21 (10): 4171—4175. doi:10.1111/jocd.14773. PMID 35032336. S2CID 253239337.
- ↑ 1 2 Randolph JF (December 2018). "Gender-Affirming Hormone Therapy for Transgender Females". Clin Obstet Gynecol. 61 (4): 705—721. doi:10.1097/GRF.0000000000000396. PMID 30256230. S2CID 52821192.
- ↑ 1 2 3 Edndocrinology: Adult and Pediatric. — Elsevier Health Sciences, 25 February 2015. — P. 2425–2426, 2139. — ISBN 978-0-323-32195-2.
- ↑ 1 2 Yuan J, Desouza R, Westney OL, Wang R (2008). "Insights of priapism mechanism and rationale treatment for recurrent priapism". Asian Journal of Andrology. 10 (1): 88—101. doi:10.1111/j.1745-7262.2008.00314.x. PMID 18087648.
- ↑ 1 2 Elliott S, Latini DM, Walker LM, Wassersug R, Robinson JW (2010). "Androgen deprivation therapy for prostate cancer: recommendations to improve patient and partner quality of life". The Journal of Sexual Medicine. 7 (9): 2996—3010. doi:10.1111/j.1743-6109.2010.01902.x. PMID 20626600.
- ↑ 1 2 Androgen Deprivation Therapy for Advanced Prostate Cancer // Urologic Oncology. — Springer International Publishing, 2019. — P. 255–276. — «Bicalutamide is the most widely used antiandrogen in the treatment of prostate cancer. [...] Common side effects [of bicalutamide] include breast enlargement, breast tenderness, hot flashes, and constipation as well as feminization and changes in mood and liver as well as lung toxicity; monitoring of liver enzymes is recommended during treatment (Schellhammer and Davis 2004).». — ISBN 978-3-319-42622-8. — doi:10.1007/978-3-319-42623-5_77.
- ↑ Management of Urological Cancers in Older People. — Springer Science & Business Media, 2 October 2012. — P. 84–. — ISBN 978-0-85729-986-4.
- ↑ 1 2 Hair Disorders: Current Concepts in Pathophysiology, Diagnosis and Management, An Issue of Dermatologic Clinics. — Elsevier Health Sciences, 12 November 2012. — P. 187–. — ISBN 978-1-4557-7169-1.
- ↑ 1 2 Jia AY, Spratt DE (June 2022). "Bicalutamide Monotherapy With Radiation Therapy for Localized Prostate Cancer: A Non-Evidence-Based Alternative". Int J Radiat Oncol Biol Phys. 113 (2): 316—319. doi:10.1016/j.ijrobp.2022.01.037. PMID 35569476. S2CID 248765294.
Four other randomized trials using BICmono have also raised concerns about either lack of efficacy or even harm from this treatment approach compared with placebo or no hormone therapy. SPCG-6 randomized 1218 patients to either 150 mg of BICmono daily or placebo. In the subset of patients with LPCa managed with observation, survival was significantly worse with BIC than placebo (hazard ratio [HR], 1.47; 95% confidence interval, 1.06-2.03).10 Two other randomized trials were part of the early prostate cancer program,11 which conducted 3 randomized trials that were pooled together to determine the benefit of BICmono (SPCG-6 was one of the 3 trials). Overall, in the combined 8113 patient pooled cohort, after a median follow-up of 7 years, there was no improvement even in progression-free survival from the use of adjuvant BIC in LPCa, and there was a trend for worse overall survival (HR, 1.16; 95% confidence interval, 0.99-1.37; P = .07). [...] Although not in LPCa, NRG/RTOG 9601 demonstrated findings consistent with the prior trials.12 This trial randomized men to postprostatectomy salvage radiation therapy plus placebo versus 150 mg of BICmono daily for 2 years. After a median follow-up of 13 years, the trial showed that there were significantly more grade 3 to 5 cardiac events in the BICmono arm. In patients with less aggressive disease with lower PSAs (prostate-specific antigens; more analogous to LPCa), other-cause mortality was significantly higher in the BICmono arm. In patients with high PSAs >1.5 ng/mL (which with modern molecular positron emission tomography imaging would be expected to have high rates of regional and distant metastatic disease), a survival benefit from the addition of BIC was observed. This is consistent with results from the early prostate cancer studies that showed that only patients with more advanced disease derived benefit from BICmono.10 Thus, all the randomized evidence from 5 trials (Table 1) demonstrates that, in LPCa, BICmono had no clinically significant oncologic activity over placebo/no treatment, and consistent trends with long-term use resulted in worse survival.
- ↑ 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 Casodex- bicalutamide tablet. DailyMed (1 сентября 2019). Дата обращения: 7 мая 2020. Архивировано 27 июля 2020 года.
- ↑ 1 2 Lee K, Oda Y, Sakaguchi M, Yamamoto A, Nishigori C (May 2016). "Drug-induced photosensitivity to bicalutamide – case report and review of the literature". Photodermatology, Photoimmunology & Photomedicine. 32 (3): 161—4. doi:10.1111/phpp.12230. PMID 26663090. S2CID 2761388.
- ↑ Lee K, et al. (2016). "Drug-induced photosensitivity to bicalutamide – case report and review of the literature". Reactions Weekly. 1612 (1): 161—4. doi:10.1007/s40278-016-19790-1. PMID 26663090. S2CID 261402820.
- ↑ 1 2 Singh SM, Gauthier S, Labrie F (February 2000). "Androgen receptor antagonists (antiandrogens): structure-activity relationships". Current Medicinal Chemistry. 7 (2): 211—47. doi:10.2174/0929867003375371. PMID 10637363.
- ↑ 1 2 Yen & Jaffe's Reproductive Endocrinology: Physiology, Pathophysiology, and Clinical Management. — Elsevier Health Sciences, 28 August 2013. — P. 688–. — «Bone density improves in men receiving bicalutamide, most likely secondary to the 146% increase in estradiol and the fact that estradiol is the major mediator of bone density in men.». — ISBN 978-1-4557-5972-9.
- ↑ 1 2 3 Osteoporosis. — Academic Press, 8 November 2007. — P. 1354–. — ISBN 978-0-08-055347-4.
- ↑ 1 2 3 4 5 Mahler C, Verhelst J, Denis L (May 1998). "Clinical pharmacokinetics of the antiandrogens and their efficacy in prostate cancer". Clinical Pharmacokinetics. 34 (5): 405—17. doi:10.2165/00003088-199834050-00005. PMID 9592622. S2CID 25200595.
- ↑ 1 2 3 4 5 Furr BJ, Tucker H (January 1996). "The preclinical development of bicalutamide: pharmacodynamics and mechanism of action". Urology. 47 (1A Suppl): 13—25, discussion 29–32. doi:10.1016/S0090-4295(96)80003-3. PMID 8560673.
- ↑ Analogue-based Drug Discovery : [англ.]. — John Wiley & Sons, 2006. — P. 515. — ISBN 9783527607495.
- ↑ World Health Organization model list of essential medicines: 21st list 2019. — Geneva : World Health Organization, 2019. — ISBN WHO/MVP/EMP/IAU/2019.06. License: CC BY-NC-SA 3.0 IGO.
- ↑ Tarascon Pocket Pharmacopoeia 2015 Deluxe Lab-Coat Edition. — Jones & Bartlett Learning, 2015. — P. 381. — ISBN 9781284057560.
- ↑ 1 2 3 4 5 6 7 8 Bicalutamide – International Drug Names. Drugs.com. Дата обращения: 13 августа 2016. Архивировано 18 сентября 2016 года.
- ↑ 1 2 Akaza H (1999). "[A new anti-androgen, bicalutamide (Casodex), for the treatment of prostate cancer—basic clinical aspects]". Gan to Kagaku Ryoho. Cancer & Chemotherapy (яп.). 26 (8): 1201—7. PMID 10431591.
- ↑ 1 2 3 4 1999 Annual Report and Form 20-F. AstraZeneca. Дата обращения: 1 июля 2017. Архивировано 9 сентября 2017 года.
- ↑ Mukherji D, Pezaro CJ, De-Bono JS (February 2012). "MDV3100 for the treatment of prostate cancer". Expert Opinion on Investigational Drugs. 21 (2): 227—33. doi:10.1517/13543784.2012.651125. PMID 22229405. S2CID 46339544.
- ↑ Pchejetski D, Alshaker H, Stebbing J (2014). "Castrate-resistant prostate cancer: the future of antiandrogens" (PDF). Trends in Urology & Men's Health. 5 (1): 7—10. doi:10.1002/tre.371. S2CID 57988002. Архивировано (PDF) 19 июля 2018. Дата обращения: 11 декабря 2019.
- ↑ 1 2 3 4 Slowing Sales for Johnson & Johnson's Zytiga May Be Good News for Medivation. The Motley Fool (22 января 2014). — «[...] the most commonly prescribed treatment for metastatic castration resistant prostate cancer: bicalutamide. That was sold as AstraZeneca's billion-dollar-a-year drug Casodex before losing patent protection in 2008. AstraZeneca still generates a few hundred million dollars in sales from Casodex, [...]». Дата обращения: 20 июля 2016. Архивировано 26 августа 2016 года.
- ↑ 1 2 3 4 5 6 https://www.fda.gov/downloads/AdvisoryCommittees/CommitteesMeetingMaterials/PediatricAdvisoryCommittee/UCM214400.pdf
{{citation}}:|title=пропущен или пуст (справка)Википедия:Обслуживание CS1 (url-status) (ссылка) - ↑ 1 2 Androgens in Health and Disease. — Springer Science & Business Media, 27 May 2003. — P. 25–. — ISBN 978-1-59259-388-0.
- ↑ Klotz L, Schellhammer P (March 2005). "Combined androgen blockade: the case for bicalutamide". Clinical Prostate Cancer. 3 (4): 215—9. doi:10.3816/cgc.2005.n.002. PMID 15882477.
- ↑ Schellhammer PF, Sharifi R, Block NL, Soloway MS, Venner PM, Patterson AL, Sarosdy MF, Vogelzang NJ, Schellenger JJ, Kolvenbag GJ (September 1997). "Clinical benefits of bicalutamide compared with flutamide in combined androgen blockade for patients with advanced prostatic carcinoma: final report of a double-blind, randomized, multicenter trial. Casodex Combination Study Group". Urology. 50 (3): 330—6. doi:10.1016/S0090-4295(97)00279-3. PMID 9301693.
- ↑ 1 2 3 Suzuki H, Kamiya N, Imamoto T, Kawamura K, Yano M, Takano M, Utsumi T, Naya Y, Ichikawa T (October 2008). "Current topics and perspectives relating to hormone therapy for prostate cancer". International Journal of Clinical Oncology. 13 (5): 401—10. doi:10.1007/s10147-008-0830-y. PMID 18946750. S2CID 32859879.
- ↑ 1 2 Usami M, Akaza H, Arai Y, Hirano Y, Kagawa S, Kanetake H, Naito S, Sumiyoshi Y, Takimoto Y, Terai A, Yoshida H, Ohashi Y (2007). "Bicalutamide 80 mg combined with a luteinizing hormone-releasing hormone agonist (LHRH-A) versus LHRH-A monotherapy in advanced prostate cancer: findings from a phase III randomized, double-blind, multicenter trial in Japanese patients". Prostate Cancer Prostatic Dis. 10 (2): 194—201. doi:10.1038/sj.pcan.4500934. PMID 17199134.
In most countries, bicalutamide is given at a dose of 50 mg when used in combination with an LHRH-A. However, based on pharmacokinetic and pharmacodynamic data, the approved dose of bicalutamide in Japanese men is 80 mg per day.
- ↑ 1 2 Williams Textbook of Endocrinology. — Elsevier Health Sciences, 1 January 2016. — P. 752–. — «GnRH analogues, both agonists and antagonists, severely suppress endogenous gonadotropin and testosterone production [...] Administration of GnRH agonists (e.g., leuprolide, goserelin) produces an initial stimulation of gonadotropin and testosterone secretion (known as a "flare"), which is followed in 1 to 2 weeks by GnRH receptor downregulation and marked suppression of gonadotropins and testosterone to castration levels. [...] To prevent the potential complications associated with the testosterone flare, AR antagonists (e.g., bicalutamide) are usually coadministered with a GnRH agonist for men with metastatic prostate cancer.399». — ISBN 978-0-323-29738-7.
- ↑ Sugiono M, Winkler MH, Okeke AA, Benney M, Gillatt DA (2005). "Bicalutamide vs cyproterone acetate in preventing flare with LHRH analogue therapy for prostate cancer—a pilot study". Prostate Cancer and Prostatic Diseases. 8 (1): 91—4. doi:10.1038/sj.pcan.4500784. PMID 15711607.
- ↑ 1 2 3 Erem C (2013). "Update on idiopathic hirsutism: diagnosis and treatment". Acta Clinica Belgica. 68 (4): 268—74. doi:10.2143/ACB.3267. PMID 24455796. S2CID 39120534.
- ↑ Ascenso A, Marques HC (January 2009). "Acne in the adult". Mini Reviews in Medicinal Chemistry. 9 (1): 1—10. doi:10.2174/138955709787001730. PMID 19149656.
- ↑ Kaur S, Verma P, Sangwan A, Dayal S, Jain VK (2016). "Etiopathogenesis and Therapeutic Approach to Adult Onset Acne". Indian Journal of Dermatology. 61 (4): 403—7. doi:10.4103/0019-5154.185703. PMC 4966398. PMID 27512185.
- ↑ Hormonal Treatment for Skin Androgen-Related Disorders // European Handbook of Dermatological Treatments. — 2015. — P. 1451–1464. — ISBN 978-3-662-45138-0. — doi:10.1007/978-3-662-45139-7_142.
- ↑ Müderris II, Öner G (2009). "Hirsutizm Tedavisinde Flutamid ve Bikalutamid Kullanımı" [Flutamide and Bicalutamide Treatment in Hirsutism]. Turkiye Klinikleri Journal of Endocrinology-Special Topics (тур.). 2 (2): 110—2. ISSN 1304-0529. Архивировано 27 июля 2020. Дата обращения: 28 марта 2019.
- ↑ 1 2 3 Moretti C, Guccione L, Di Giacinto P, Simonelli I, Exacoustos C, Toscano V, Motta C, De Leo V, Petraglia F, Lenzi A (March 2018). "Combined Oral Contraception and Bicalutamide in Polycystic Ovary Syndrome and Severe Hirsutism: A Double-Blind Randomized Controlled Trial". J. Clin. Endocrinol. Metab. 103 (3): 824—838. doi:10.1210/jc.2017-01186. PMID 29211888.
- ↑ Endocrine Care of Transgender Adults // Transgender Medicine. — 2019. — P. 143–163. — ISBN 978-3-030-05682-7. — doi:10.1007/978-3-030-05683-4_8.
- ↑ Neyman A, Fuqua JS, Eugster EA (April 2019). "Bicalutamide as an Androgen Blocker With Secondary Effect of Promoting Feminization in Male-to-Female Transgender Adolescents". The Journal of Adolescent Health. 64 (4): 544—546. doi:10.1016/j.jadohealth.2018.10.296. PMC 6431559. PMID 30612811.
- ↑ Gooren LJ (March 2011). "Clinical practice. Care of transsexual persons". The New England Journal of Medicine. 364 (13): 1251—1257. doi:10.1056/nejmcp1008161. PMID 21449788.
- ↑ Guidelines for the Primary and Gender-Affirming Care of Transgender and Gender Nonbinary People. — 2nd. — University of California, San Francisco : Center of Excellence for Transgender Health, 17 June 2016. — P. 28.
- ↑ Transgender Health: A Practitioner's Guide to Binary and Non-Binary Trans Patient Care. — Jessica Kingsley Publishers, 21 June 2018. — P. 158–. — ISBN 978-1-78450-475-5.
- ↑ 1 2 Wierckx K, Gooren L, T'Sjoen G (May 2014). "Clinical review: Breast development in trans women receiving cross-sex hormones". The Journal of Sexual Medicine. 11 (5): 1240—1247. doi:10.1111/jsm.12487. PMID 24618412.
- ↑ Treatment of Peripheral Precocious Puberty // Puberty from Bench to Clinic. — 2015. — Vol. 29. — P. 230–239. — ISBN 978-3-318-02788-4. — doi:10.1159/000438895.
- ↑ Haddad NG, Eugster EA (June 2019). "Peripheral precocious puberty including congenital adrenal hyperplasia: causes, consequences, management and outcomes". Best Practice & Research. Clinical Endocrinology & Metabolism. 33 (3): 101273. doi:10.1016/j.beem.2019.04.007. PMID 31027974. S2CID 135410503.
{{cite journal}}:|hdl-access=требует|hdl=(справка) - ↑ Peripheral Precocious Puberty: Interventions to Improve Growth // Handbook of Growth and Growth Monitoring in Health and Disease. — 2012. — P. 1199–1212. — ISBN 978-1-4419-1794-2. — doi:10.1007/978-1-4419-1795-9_71.
- ↑ Disorders of Puberty: Pharmacotherapeutic Strategies for Management // Pediatric Pharmacotherapy. — 2019. — Vol. 261. — P. 507–538. — ISBN 978-3-030-50493-9. — doi:10.1007/164_2019_208.
- ↑ Nelson Textbook of Pediatrics. — Elsevier Health Sciences, 17 April 2015. — P. 2661–. — ISBN 978-0-323-26352-8.
- ↑ Reiter EO, Mauras N, McCormick K, Kulshreshtha B, Amrhein J, De Luca F, et al. (October 2010). "Bicalutamide plus anastrozole for the treatment of gonadotropin-independent precocious puberty in boys with testotoxicosis: a phase II, open-label pilot study (BATT)". Journal of Pediatric Endocrinology & Metabolism. 23 (10): 999—1009. doi:10.1515/jpem.2010.161. PMID 21158211. S2CID 110630.
- ↑ Levey HR, Kutlu O, Bivalacqua TJ (January 2012). "Medical management of ischemic stuttering priapism: a contemporary review of the literature". Asian Journal of Andrology. 14 (1): 156—163. doi:10.1038/aja.2011.114. PMC 3753435. PMID 22057380.
- ↑ Broderick GA, Kadioglu A, Bivalacqua TJ, Ghanem H, Nehra A, Shamloul R (January 2010). "Priapism: pathogenesis, epidemiology, and management". The Journal of Sexual Medicine. 7 (1 Pt 2): 476—500. doi:10.1111/j.1743-6109.2009.01625.x. PMID 20092449.
- ↑ Chow K, Payne S (December 2008). "The pharmacological management of intermittent priapismic states". BJU International. 102 (11): 1515—1521. doi:10.1111/j.1464-410X.2008.07951.x. PMID 18793304. S2CID 35399393.
- ↑ Dahm P, Rao DS, Donatucci CF (January 2002). "Antiandrogens in the treatment of priapism". Urology. 59 (1): 138. doi:10.1016/S0090-4295(01)01492-3. PMID 11796309.
- ↑ Gooren LJ (2011). "Clinical review: Ethical and medical considerations of androgen deprivation treatment of sex offenders". The Journal of Clinical Endocrinology & Metabolism. 96 (12): 3628—37. doi:10.1210/jc.2011-1540. PMID 21956411.
- ↑ Giltay EJ, Gooren LJ (2009). "Potential side effects of androgen deprivation treatment in sex offenders". The Journal of the American Academy of Psychiatry and the Law. 37 (1): 53—8. PMID 19297634.
- ↑ Khan O, Mashru A (2016). "The efficacy, safety and ethics of the use of testosterone-suppressing agents in the management of sex offending". Current Opinion in Endocrinology, Diabetes and Obesity. 23 (3): 271—8. doi:10.1097/MED.0000000000000257. PMID 27032060. S2CID 43286710.
- ↑ Dangerous Sex Offenders: A Task Force Report of the American Psychiatric Association. — American Psychiatric Pub, 1999. — P. 111–. — ISBN 978-0-89042-280-9.
- ↑ Houts FW, Taller I, Tucker DE, Berlin FS (2011). "Androgen deprivation treatment of sexual behavior". Advances in Psychosomatic Medicine. 31: 149—63. doi:10.1159/000330196. ISBN 978-3-8055-9825-5. PMID 22005210.
- ↑ Rousseau L, Couture M, Dupont A, Labrie F, Couture N (1990). "Effect of combined androgen blockade with an LHRH agonist and flutamide in one severe case of male exhibitionism". The Canadian Journal of Psychiatry. 35 (4): 338—41. doi:10.1177/070674379003500412. PMID 2189544. S2CID 28970865.
- ↑ 1 2 3 4 5 Index Nominum 2000: International Drug Directory / Swiss Pharmaceutical Society. — Taylor & Francis, January 2000. — P. 123–. — ISBN 978-3-88763-075-1.
- ↑ 1 2 3 Martindale: The Complete Drug Reference. — Pharmaceutical Press, 2011. — P. 750–751. — ISBN 978-0-85369-933-0.
- ↑ 1 2 Handbook of Drug Administration via Enteral Feeding Tubes. — 3rd. — Pharmaceutical Press, 11 March 2015. — P. 133–. — ISBN 978-0-85711-162-3.
- ↑ 1 2 The Avery Complete Guide to Medicines. — Avery, 2001. — P. 105–106. — ISBN 978-1-58333-105-7.
- ↑ 1 2 3 4 5 Cancer Chemotherapy and Biotherapy: Principles and Practice. — Lippincott Williams & Wilkins, 8 November 2010. — P. 679–680. — «From a structural standpoint, antiandrogens are classified as steroidal, including cyproterone [acetate] (Androcur) and megestrol [acetate], or nonsteroidal, including flutamide (Eulexin, others), bicalutamide (Casodex), and nilutamide (Nilandron). The steroidal antiandrogens are rarely used.». — ISBN 978-1-60547-431-1.
- ↑ Kolvenbag GJ, Furr BJ, Blackledge GR (December 1998). "Receptor affinity and potency of non-steroidal antiandrogens: translation of preclinical findings into clinical activity". Prostate Cancer Prostatic Dis. 1 (6): 307—314. doi:10.1038/sj.pcan.4500262. PMID 12496872. S2CID 33497597.
In addition, since bicalutamide has a low solubility, authentic Casodex® is micronised to ensure a small and consistent particle size to optimise bioavailability.
- ↑ 1 2 Zolacos CP. Drugs.com. Архивировано 20 сентября 2016 года.
- ↑ 1 2 Zolacos CP. MIMS/myDr (апрель 2007). Архивировано из оригинала 17 сентября 2016 года.
- ↑ 1 2 ZOLACOS CP. New Zealand Data Sheet (25 июля 2016). Архивировано 19 сентября 2016 года.
- ↑ 1 2 3 4 5 6 7 COSUDEX® (bicalutamide) 150 mg tablets. TGA. Архивировано 14 сентября 2016 года.
- ↑ 1 2 3 Iswaran TJ, Imai M, Betton GR, Siddall RA (May 1997). "An overview of animal toxicology studies with bicalutamide (ICI 176,334)". The Journal of Toxicological Sciences. 22 (2): 75—88. doi:10.2131/jts.22.2_75. PMID 9198005.
- ↑ 1 2 Medicinal Chemistry – Fusion of Traditional and Western Medicine. — Bentham Science Publishers, 4 April 2013. — P. 306–. — ISBN 978-1-60805-149-6.
- ↑ Handbook of Cancer Chemotherapy. — Lippincott Williams & Wilkins, 2011. — P. 724–. — ISBN 9781608317820.
- ↑ Mosby's GenRx: A Comprehensive Reference for Generic and Brand Prescription Drugs. — Mosby, 2001. — P. 289–290. — ISBN 978-0-323-00629-3.
- ↑ Physicians' Desk Reference. — Thomson PDR, 2004. — ISBN 978-1-56363-471-0.
- ↑ 1 2 3 4 Pharmacology for Nursing Care. — Elsevier Health Sciences, 2013. — P. 1297–. — ISBN 978-1-4377-3582-6.
- ↑ 1 2 3 4 Wirth MP, Hakenberg OW, Froehner M (February 2007). "Antiandrogens in the treatment of prostate cancer". European Urology. 51 (2): 306—13, discussion 314. doi:10.1016/j.eururo.2006.08.043. PMID 17007995.
- ↑ 1 2 3 4 5 6 Wellington K, Keam SJ (2006). "Bicalutamide 150mg: a review of its use in the treatment of locally advanced prostate cancer". Drugs. 66 (6): 837—50. doi:10.2165/00003495-200666060-00007. PMID 16706554. S2CID 46966712.
- ↑ Higano CS (February 2003). "Side effects of androgen deprivation therapy: monitoring and minimizing toxicity". Urology. 61 (2 Suppl 1): 32—8. doi:10.1016/S0090-4295(02)02397-X. PMID 12667885.
- ↑ Higano CS (2012). "Sexuality and intimacy after definitive treatment and subsequent androgen deprivation therapy for prostate cancer". Journal of Clinical Oncology. 30 (30): 3720—5. doi:10.1200/JCO.2012.41.8509. PMID 23008326.
- ↑ 1 2 3 4 5 6 7 8 Kolvenbag GJ, Blackledge GR (January 1996). "Worldwide activity and safety of bicalutamide: a summary review". Urology. 47 (1A Suppl): 70—9, discussion 80–4. doi:10.1016/s0090-4295(96)80012-4. PMID 8560681.
Bicalutamide is a new antiandrogen that offers the convenience of once-daily administration, demonstrated activity in prostate cancer, and an excellent safety profile. Because it is effective and offers better tolerability than flutamide, bicalutamide represents a valid first choice for antiandrogen therapy in combination with castration for the treatment of patients with advanced prostate cancer.
- ↑ Advanced Therapy of Prostate Disease. — PMPH-USA, 2000. — P. 379–. — ISBN 978-1-55009-102-1.
- ↑ 1 2 3 4 5 Iversen P, Melezinek I, Schmidt A (January 2001). "Nonsteroidal antiandrogens: a therapeutic option for patients with advanced prostate cancer who wish to retain sexual interest and function". BJU International. 87 (1): 47—56. doi:10.1046/j.1464-410x.2001.00988.x. PMID 11121992. S2CID 28215804.
- ↑ 1 2 3 4 5 6 7 Anderson J (March 2003). "The role of antiandrogen monotherapy in the treatment of prostate cancer". BJU Int. 91 (5): 455—61. doi:10.1046/j.1464-410X.2003.04026.x. PMID 12603397. S2CID 8639102.
- ↑ Kathryn Korkidakis A, Reid RL (2017). "Testosterone in Women: Measurement and Therapeutic Use". Journal of Obstetrics and Gynaecology Canada. 39 (3): 124—130. doi:10.1016/j.jogc.2017.01.006. PMID 28343552.
- ↑ Davis SR, Wahlin-Jacobsen S (2015). "Testosterone in women--the clinical significance". The Lancet Diabetes & Endocrinology. 3 (12): 980—92. doi:10.1016/S2213-8587(15)00284-3. PMID 26358173.
- ↑ Cignarella A, Mioni R, Sabbadin C, Dassie F, Parolin M, Vettor R, Barbot M, Scaroni C (December 2020). "Pharmacological Approaches to Controlling Cardiometabolic Risk in Women with PCOS". Int J Mol Sci. 21 (24): 9554. doi:10.3390/ijms21249554. PMC 7765466. PMID 33334002.
- ↑ Luque-Ramírez M, Ortiz-Flores AE, Nattero-Chávez L, Escobar-Morreale HF (December 2020). "A safety evaluation of current medications for adult women with the polycystic ovarian syndrome not pursuing pregnancy". Expert Opin Drug Saf. 19 (12): 1559—1576. doi:10.1080/14740338.2020.1839409. PMID 33070640. S2CID 224784192.
- ↑ Fourcade RO, McLeod D (March 2004). "Tolerability of Antiandrogens in the Treatment of Prostate Cancer". UroOncology. 4 (1): 5—13. doi:10.1080/1561095042000191655. ISSN 1561-0950.
Based on the available evidence, bicalutamide appears to have a better profile of non-pharmacological side effects than either flutamide or nilutamide; no specific nonpharmacological complications have yet been linked to this agent, while the incidence of the side effects such as diarrhoea and abnormal liver function appears to be lower than for the other two non-steroidal compounds. Furthermore, the recent data from the EPC programme suggest that the non-pharmacological side-effect profile of bicalutamide is not dissimilar to that of placebo (Table m [3].
- ↑ Lunglmayr G (August 1995). "Efficacy and tolerability of Casodex in patients with advanced prostate cancer. International Casodex Study Group". Anti-Cancer Drugs. 6 (4): 508—13. doi:10.1097/00001813-199508000-00003. PMID 7579554.
- ↑ McLeod DG (1997). "Tolerability of Nonsteroidal Antiandrogens in the Treatment of Advanced Prostate Cancer". Oncologist. 2 (1): 18—27. doi:10.1634/theoncologist.2-1-18. PMID 10388026.
- ↑ Neurologic Complications of Cancer. — Oxford University Press, USA, 12 September 2008. — P. 479–. — ISBN 978-0-19-971055-3.
- ↑ Canadian Guide to Prostate Cancer. — John Wiley & Sons, 5 November 2012. — P. 177–. — ISBN 978-1-118-51565-5.
- ↑ Tyrrell CJ, Denis L, Newling D, Soloway M, Channer K, Cockshott ID (1998). "Casodex 10-200 mg daily, used as monotherapy for the treatment of patients with advanced prostate cancer. An overview of the efficacy, tolerability and pharmacokinetics from three phase II dose-ranging studies. Casodex Study Group". Eur. Urol. 33 (1): 39—53. doi:10.1159/000019526. PMID 9471040. S2CID 71758492. Архивировано 1 февраля 2022. Дата обращения: 13 апреля 2023.
- ↑ 1 2 3 4 Tyrrell CJ, Iversen P, Tammela T, Anderson J, Björk T, Kaisary AV, Morris T (September 2006). "Tolerability, efficacy and pharmacokinetics of bicalutamide 300 mg, 450 mg or 600 mg as monotherapy for patients with locally advanced or metastatic prostate cancer, compared with castration". BJU International. 98 (3): 563—72. doi:10.1111/j.1464-410X.2006.06275.x. PMID 16771791. S2CID 41672303.
- ↑ 1 2 See WA, Wirth MP, McLeod DG, Iversen P, Klimberg I, Gleason D, et al. (August 2002). "Bicalutamide as immediate therapy either alone or as adjuvant to standard care of patients with localized or locally advanced prostate cancer: first analysis of the early prostate cancer program". The Journal of Urology. 168 (2): 429—35. doi:10.1016/S0022-5347(05)64652-6. PMID 12131282.
- ↑ Schellhammer P, Sharifi R, Block N, Soloway M, Venner P, Patterson AL, Sarosdy M, Vogelzang N, Jones J, Kolvenbag G (January 1996). "Maximal androgen blockade for patients with metastatic prostate cancer: outcome of a controlled trial of bicalutamide versus flutamide, each in combination with luteinizing hormone-releasing hormone analogue therapy. Casodex Combination Study Group". Urology. 47 (1A Suppl): 54—60, discussion 80–4. doi:10.1016/s0090-4295(96)80010-0. PMID 8560679.
- ↑ Iversen P, Johansson JE, Lodding P, Lukkarinen O, Lundmo P, Klarskov P, Tammela TL, Tasdemir I, Morris T, Carroll K (November 2004). "Bicalutamide (150 mg) versus placebo as immediate therapy alone or as adjuvant to therapy with curative intent for early nonmetastatic prostate cancer: 5.3-year median followup from the Scandinavian Prostate Cancer Group Study Number 6". The Journal of Urology. 172 (5 Pt 1): 1871—6. doi:10.1097/01.ju.0000139719.99825.54. PMID 15540741.
- ↑ Wellington K, Keam SJ (2006). "Bicalutamide 150mg: a review of its use in the treatment of locally advanced prostate cancer". Drugs. 66 (6): 837—50. doi:10.2165/00003495-200666060-00007. PMID 16706554. S2CID 46966712.
- ↑ Iversen P, Johansson JE, Lodding P, Kylmälä T, Lundmo P, Klarskov P, Tammela TL, Tasdemir I, Morris T, Armstrong J (2006). "Bicalutamide 150 mg in addition to standard care for patients with early non-metastatic prostate cancer: updated results from the Scandinavian Prostate Cancer Period Group-6 Study after a median follow-up period of 7.1 years". Scandinavian Journal of Urology and Nephrology. 40 (6): 441—52. doi:10.1080/00365590601017329. PMID 17130095. S2CID 25862814.
- ↑ 1 2 Trüeb RM, Luu NC, Uribe NC, Régnier A (December 2022). "Comment on: Bicalutamide and the new perspectives for female pattern hair loss treatment: What dermatologists should know". J Cosmet Dermatol. 21 (12): 7200—7201. doi:10.1111/jocd.14936. PMID 35332669. S2CID 247677549.
Indeed, due to the minimal biological importance of androgens in women, the adverse effects of bicalutamide are few. And yet, bicalutamide has been associated with elevated liver enzymes, and as of 2021, there have been 10 case reports of liver toxicity associated with bicalutamide, with fatality occurring in 2 cases.2
- ↑ 1 2 Gretarsdottir HM, Bjornsdottir E, Bjornsson ES (2018). "Bicalutamide-Associated Acute Liver Injury and Migratory Arthralgia: A Rare but Clinically Important Adverse Effect". Case Reports in Gastroenterology. 12 (2): 266—70. doi:10.1159/000485175. ISSN 1662-0631.
{{cite journal}}:|hdl-access=требует|hdl=(справка) - ↑ 1 2 3 Hussain S, Haidar A, Bloom RE, Zayouna N, Piper MH, Jafri SM (2014). "Bicalutamide-induced hepatotoxicity: A rare adverse effect". Am J Case Rep. 15: 266—70. doi:10.12659/AJCR.890679. PMC 4068966. PMID 24967002.
- ↑ 1 2 Yun GY, Kim SH, Kim SW, Joo JS, Kim JS, Lee ES, Lee BS, Kang SH, Moon HS, Sung JK, Lee HY, Kim KH (April 2016). "Atypical onset of bicalutamide-induced liver injury". World J. Gastroenterol. 22 (15): 4062—5. doi:10.3748/wjg.v22.i15.4062. PMC 4823258. PMID 27099451.
- ↑ 1 2 O'Bryant CL, Flaig TW, Utz KJ (2008). "Bicalutamide-associated fulminant hepatotoxicity". Pharmacotherapy. 28 (8): 1071—5. doi:10.1592/phco.28.8.1071. PMID 18657023. S2CID 20315801.
- ↑ Castro Beza I, Sánchez Ruiz J, Peracaula Espino FJ, Villanego Beltrán MI (September 2008). "Drug-related hepatotoxicity and hepatic failure following combined androgen blockade". Clin Transl Oncol. 10 (9): 591—2. doi:10.1007/s12094-008-0256-5. PMID 18796378.
- ↑ 1 2 "FDA Adverse Event Reporting System (FAERS) Public Dashboard". FDA. 22 October 2021. Архивировано 15 февраля 2023. Дата обращения: 15 февраля 2023.
- ↑ Medical Toxicology. — Lippincott Williams & Wilkins, 2004. — P. 497–. — ISBN 978-0-7817-2845-4.
- ↑ Masago T, Watanabe T, Nemoto R, Motoda K (December 2011). "Interstitial pneumonitis induced by bicalutamide given for prostate cancer". International Journal of Clinical Oncology. 16 (6): 763—5. doi:10.1007/s10147-011-0239-x. PMID 21537882. S2CID 24068787.
- ↑ Side Effects of Drugs Annual: A worldwide yearly survey of new data in adverse drug reactions. — Newnes, 4 March 2014. — P. 740–. — ISBN 978-0-444-62636-3.
- ↑ Daba MH, El-Tahir KE, Al-Arifi MN, Gubara OA (June 2004). "Drug-induced pulmonary fibrosis". Saudi Medical Journal. 25 (6): 700—6. PMID 15195196.
- ↑ Thole Z, Manso G, Salgueiro E, Revuelta P, Hidalgo A (2004). "Hepatotoxicity induced by antiandrogens: a review of the literature". Urologia Internationalis. 73 (4): 289—95. doi:10.1159/000081585. PMID 15604569. S2CID 24799765.
- ↑ Ricci F, Buzzatti G, Rubagotti A, Boccardo F (November 2014). "Safety of antiandrogen therapy for treating prostate cancer". Expert Opinion on Drug Safety. 13 (11): 1483—99. doi:10.1517/14740338.2014.966686. PMID 25270521. S2CID 207488100.
- ↑ Sex Differences in the Human Brain, their underpinnings and implications. — Elsevier, 3 December 2010. — P. 44–45. — ISBN 978-0-444-53631-0.
- ↑ Chemistry and Brain Development: Proceedings of the Advanced Study Institute on "Chemistry of Brain Development," held in Milan, Italy, September 9–19, 1970. — Springer Science & Business Media, 6 December 2012. — P. 218–. — ISBN 978-1-4684-7236-3.
- ↑ The challenging role of antiandrogens in the management of polycystic ovary syndrome // Polycystic Ovary Syndrome. — Elsevier, 2022. — P. 297–314. — ISBN 9780128230459. — doi:10.1016/B978-0-12-823045-9.00013-4.
- ↑ Prostate Cancer. — Springer Science & Business Media, 5 June 2007. — P. 256–. — ISBN 978-3-540-40901-4.
- ↑ Controversies in the Treatment of Prostate Cancer. — Karger Medical and Scientific Publishers, 1 January 2008. — P. 41–. — ISBN 978-3-8055-8524-8.
- ↑ Prostate Cancer. — Demos Medical Publishing, 20 December 2011. — P. 504–505. — ISBN 978-1-935281-91-7.
- ↑ 1 2 3 4 Meyler's Side Effects of Endocrine and Metabolic Drugs. — Elsevier, 21 February 2009. — P. 149–150, 253–258. — ISBN 978-0-08-093292-7.
- ↑ Transsexual and Other Disorders of Gender Identity: A Practical Guide to Management. — Radcliffe Publishing, 2007. — P. 174–. — ISBN 978-1-85775-719-4.
- ↑ Rushton DH (2002). "Nutritional factors and hair loss". Clin. Exp. Dermatol. 27 (5): 396—404. doi:10.1046/j.1365-2230.2002.01076.x. PMID 12190640. S2CID 39327815.
- ↑ Boccardo F (2000). "Hormone therapy of prostate cancer: is there a role for antiandrogen monotherapy?". Crit. Rev. Oncol. Hematol. 35 (2): 121—32. doi:10.1016/s1040-8428(00)00051-2. PMID 10936469.
- ↑ Thole Z, Manso G, Salgueiro E, Revuelta P, Hidalgo A (2004). "Hepatotoxicity induced by antiandrogens: a review of the literature". Urol. Int. 73 (4): 289—95. doi:10.1159/000081585. PMID 15604569. S2CID 24799765.
- ↑ 1 2 Hormone Therapy in Breast and Prostate Cancer. — Springer Science & Business Media, 5 February 2010. — P. 356–. — ISBN 978-1-59259-152-7.
- ↑ Bennett CL, Raisch DW, Sartor O (October 2002). "Pneumonitis associated with nonsteroidal antiandrogens: presumptive evidence of a class effect". Annals of Internal Medicine. 137 (7): 625. doi:10.7326/0003-4819-137-7-200210010-00029. PMID 12353966.
An estimated 0.77% of the 6,480 nilutamide-treated patients, 0.04% of the 41,700 flutamide-treated patients, and 0.01% of the 86,800 bicalutamide-treated patients developed pneumonitis during the study period.
- ↑ Ricci F, Buzzatti G, Rubagotti A, Boccardo F (2014). "Safety of antiandrogen therapy for treating prostate cancer". Expert Opin Drug Saf. 13 (11): 1483—99. doi:10.1517/14740338.2014.966686. PMID 25270521. S2CID 207488100.
- ↑ Foster WR, Car BD, Shi H, Levesque PC, Obermeier MT, Gan J, Arezzo JC, Powlin SS, Dinchuk JE, Balog A, Salvati ME, Attar RM, Gottardis MM (2011). "Drug safety is a barrier to the discovery and development of new androgen receptor antagonists". Prostate. 71 (5): 480—8. doi:10.1002/pros.21263. PMID 20878947. S2CID 24620044.
- ↑ Beer TM, Armstrong AJ, Rathkopf DE, Loriot Y, Sternberg CN, Higano CS, Iversen P, Bhattacharya S, Carles J, Chowdhury S, Davis ID, de Bono JS, Evans CP, Fizazi K, Joshua AM, Kim CS, Kimura G, Mainwaring P, Mansbach H, Miller K, Noonberg SB, Perabo F, Phung D, Saad F, Scher HI, Taplin ME, Venner PM, Tombal B (2014). "Enzalutamide in metastatic prostate cancer before chemotherapy". N. Engl. J. Med. 371 (5): 424—33. doi:10.1056/NEJMoa1405095. PMC 4418931. PMID 24881730.
- ↑ Keating GM (2015). "Enzalutamide: a review of its use in chemotherapy-naïve metastatic castration-resistant prostate cancer". Drugs Aging. 32 (3): 243—9. doi:10.1007/s40266-015-0248-y. PMID 25711765. S2CID 29563345.
- ↑ Beer TM, Tombal B (2014). "Enzalutamide in metastatic prostate cancer before chemotherapy" (PDF). N. Engl. J. Med. 371 (18): 1755—6. doi:10.1056/NEJMc1410239. PMID 25354111. Архивировано (PDF) 28 августа 2021. Дата обращения: 23 сентября 2019.
{{cite journal}}:|hdl-access=требует|hdl=(справка) - ↑ Furr BJ, Tucker H (1996). "The preclinical development of bicalutamide: pharmacodynamics and mechanism of action". Urology. 47 (1A Suppl): 13—25, discussion 29–32. doi:10.1016/S0090-4295(96)80003-3. PMID 8560673.
- ↑ Lenz AM, Shulman D, Eugster EA, Rahhal S, Fuqua JS, Pescovitz OH, Lewis KA (September 2010). "Bicalutamide and third-generation aromatase inhibitors in testotoxicosis". Pediatrics. 126 (3): e728-33. doi:10.1542/peds.2010-0596. PMC 4096839. PMID 20713483.
- ↑ Greenblatt DJ, Koch-Weser J (July 1973). "Adverse reactions to spironolactone. A report from the Boston Collaborative Drug Surveillance Program". JAMA. 225 (1): 40—3. doi:10.1001/jama.1973.03220280028007. PMID 4740303.
- ↑ Handbook of Pediatric Cardiovascular Drugs. — Springer, 26 June 2014. — P. 224–. — ISBN 978-1-4471-2464-1.
- ↑ Bahceci M, Tuzcu A, Canoruc N, Tuzun Y, Kidir V, Aslan C (2004). "Serum C-reactive protein (CRP) levels and insulin resistance in non-obese women with polycystic ovarian syndrome, and effect of bicalutamide on hirsutism, CRP levels and insulin resistance". Hormone Research. 62 (6): 283—7. doi:10.1159/000081973. PMID 15542929. S2CID 46261843.
- ↑ 1 2 Nurse Practitioner's Drug Handbook. — Springhouse Corp., 2000. — ISBN 9780874349979.
- ↑ Complete Guide to Prescription & Nonprescription Drugs 2009. — HP Books, 2008. — P. 62–. — «Overdose unlikely to threaten life [with NSAAs].». — ISBN 978-0-399-53463-8.
- ↑ Genrx. 1999 Mosby's GenRx. — Mosby, 1999. — «A 79-year-old man attempted suicide by ingesting 13g of nilutamide (i.e., 43 times the maximum recommended dose). Despite immediate gastric lavage and oral administration of activated charcoal, plasma nilutamide levels peaked at 6 times the normal range 2 hours after ingestion. There were no clinical signs or symptoms or changes in parameters such as transaminases or chest x-ray. Maintenance treatment (150 mg/day) was resumed 30 days later.». — ISBN 978-0-323-00625-5.
- ↑ 1 2 3 4 5 6 7 8 9 Molecular Therapies of Cancer. — Springer, 22 July 2015. — P. 318–. — «Compared to flutamide and nilutamide, bicalutamide has a 2-fold increased affinity for the Androgen Receptor, a longer half-life, and substantially reduced toxicities. Based on a more favorable safety profile relative to flutamide, bicalutamide is indicated for use in combination therapy with a Gonadotropin Releasing Hormone analog for the treatment of advanced metastatic prostate carcinoma.». — ISBN 978-3-319-13278-5.
- ↑ Mosby's GenRx: A Comprehensive Reference for Generic and Brand Prescription Drugs. — Mosby, 2001. — P. 290. — «In vitro studies have shown bicalutamide can displace coumarin anticoagulants, such as warfarin, from their protein-binding sites. It is recommended that if bicalutamide is started in patients already receiving coumarin anticoagulants, prothrombin times should be closely monitored and adjustment of the anticoagulant dose may be necessary.». — ISBN 978-0-323-00629-3.
- ↑ 2009 Edition Delmar's Nurse's Drug Handbook. — Cengage Learning, 2 July 2008. — P. 175–. — ISBN 978-1-4283-6106-5.
- ↑ Managing Metastatic Prostate Cancer In Your Urological Oncology Practice. — Springer, 25 April 2016. — P. 24–25. — ISBN 978-3-319-31341-2.
- ↑ Masiello D, Cheng S, Bubley GJ, Lu ML, Balk SP (July 2002). "Bicalutamide functions as an androgen receptor antagonist by assembly of a transcriptionally inactive receptor". The Journal of Biological Chemistry. 277 (29): 26321—6. doi:10.1074/jbc.M203310200. PMID 12015321.
- ↑ 1 2 3 4 Antiandrogens in Prostate Cancer: A Key to Tailored Endocrine Treatment. — Springer Science & Business Media, 6 December 2012. — P. 128, 158, 203. — ISBN 978-3-642-45745-6.
- ↑ 1 2 3 Cancer Clinical Pharmacology. — OUP Oxford, 5 May 2005. — P. 229–230. — ISBN 978-0-19-262966-1.
- ↑ 1 2 3 Principles and Practice of Endocrinology and Metabolism. — Lippincott Williams & Wilkins, 2001. — P. 1119, 1196, 1208. — ISBN 978-0-7817-1750-2.
- ↑ Cancer Clinical Pharmacology. — OUP Oxford, 5 May 2005. — P. 229–230. — ISBN 978-0-19-262966-1.Schellens JH, McLeod HL, Newell DR (5 May 2005).
- ↑ Ito Y, Sadar MD (2018). "Enzalutamide and blocking androgen receptor in advanced prostate cancer: lessons learnt from the history of drug development of antiandrogens". Res Rep Urol. 10: 23—32. doi:10.2147/RRU.S157116. PMC 5818862. PMID 29497605.
- ↑ 1 2 3 Furr BJ (June 1995). "Casodex: preclinical studies and controversies". Annals of the New York Academy of Sciences. 761 (1): 79—96. Bibcode:1995NYASA.761...79F. doi:10.1111/j.1749-6632.1995.tb31371.x. PMID 7625752. S2CID 37242269.
- ↑ Guise TA, Oefelein MG, Eastham JA, Cookson MS, Higano CS, Smith MR (2007). "Estrogenic side effects of androgen deprivation therapy". Reviews in Urology. 9 (4): 163—80. PMC 2213888. PMID 18231613.
- ↑ Bulldan A, Malviya VN, Upmanyu N, Konrad L, Scheiner-Bobis G (2017). "Testosterone/bicalutamide antagonism at the predicted extracellular androgen binding site of ZIP9". Biochim. Biophys. Acta. 1864 (12): 2402—2414. doi:10.1016/j.bbamcr.2017.09.012. PMID 28943399.
- ↑ Pi M, Parrill AL, Quarles LD (2010). "GPRC6A mediates the non-genomic effects of steroids". J. Biol. Chem. 285 (51): 39953—64. doi:10.1074/jbc.M110.158063. PMC 3000977. PMID 20947496.
- ↑ Furr BJ (2009). "Research on reproductive medicine in the pharmaceutical industry". Human Fertility. 1 (1): 56—63. doi:10.1080/1464727982000198131. PMID 11844311.
- ↑ Tran C, Ouk S, Clegg NJ, Chen Y, Watson PA, Arora V, Wongvipat J, Smith-Jones PM, Yoo D, Kwon A, Wasielewska T, Welsbie D, Chen CD, Higano CS, Beer TM, Hung DT, Scher HI, Jung ME, Sawyers CL (2009). "Development of a second-generation antiandrogen for treatment of advanced prostate cancer". Science. 324 (5928): 787—90. Bibcode:2009Sci...324..787T. doi:10.1126/science.1168175. PMC 2981508. PMID 19359544.
[...] bicalutamide has relatively low affinity for AR (at least 30-fold reduced relative to the natural ligand dihydrotestosterone (DHT)) (7), [...]
- ↑ Furr BK (1997). "Relative potencies of flutamide and 'Casodex'". Endocrine-Related Cancer. 4 (2): 197—202. doi:10.1677/erc.0.0040197. ISSN 1351-0088.
- ↑ Drug Management of Prostate Cancer. — Springer Science & Business Media, 14 September 2010. — P. 56, 71–72, 75, 93. — ISBN 978-1-60327-829-4.
- ↑ Furr BJ (1996). "The development of Casodex (bicalutamide): preclinical studies". European Urology. 29 (Suppl 2): 83—95. doi:10.1159/000473846. PMID 8717469.
- ↑ 1 2 3 4 Denis L, Mahler C (January 1996). "Pharmacodynamics and pharmacokinetics of bicalutamide: defining an active dosing regimen". Urology. 47 (1A Suppl): 26—8, discussion 29–32. doi:10.1016/S0090-4295(96)80004-5. PMID 8560674.
- ↑ Boccardo F, Rubagotti A, Conti G, Potenzoni D, Manganelli A, Del Monaco D (2005). "Exploratory study of drug plasma levels during bicalutamide 150 mg therapy co-administered with tamoxifen or anastrozole for prophylaxis of gynecomastia and breast pain in men with prostate cancer". Cancer Chemotherapy and Pharmacology. 56 (4): 415—20. doi:10.1007/s00280-005-1016-1. PMID 15838655. S2CID 23014567. Архивировано 28 августа 2021. Дата обращения: 11 декабря 2019.
- ↑ Luo S, Martel C, Chen C, Labrie C, Candas B, Singh SM, Labrie F (December 1997). "Daily dosing with flutamide or Casodex exerts maximal antiandrogenic activity". Urology. 50 (6): 913—9. doi:10.1016/S0090-4295(97)00393-2. PMID 9426723.
- ↑ Williams Textbook of Endocrinology. — Elsevier Health Sciences, 30 November 2015. — P. 704–708, 711, 1104. — ISBN 978-0-323-29738-7.
- ↑ https://endo.confex.com/endo/2016endo/webprogram/Paper26631.html.
{{cite conference}}:|title=пропущен или пуст (справка)Википедия:Обслуживание CS1 (url-status) (ссылка) - ↑ Eri LM, Haug E, Tveter KJ (March 1995). "Effects on the endocrine system of long-term treatment with the non-steroidal anti-androgen Casodex in patients with benign prostatic hyperplasia". British Journal of Urology. 75 (3): 335—40. doi:10.1111/j.1464-410X.1995.tb07345.x. PMID 7537602.
- ↑ Campbell-Walsh Urology: Expert Consult Premium Edition: Enhanced Online Features and Print, 4-Volume Set. — Elsevier Health Sciences, 25 August 2011. — P. 2938–2939, 2946. — ISBN 978-1-4160-6911-9.
- ↑ 1 2 Insulin Resistance and Polycystic Ovarian Syndrome: Pathogenesis, Evaluation, and Treatment. — Springer Science & Business Media, 21 December 2009. — P. 75–. — ISBN 978-1-59745-310-3.
- ↑ 1 2 Reproductive Endocrinology and Infertility: Integrating Modern Clinical and Laboratory Practice. — Springer Science & Business Media, 23 March 2010. — P. 163–. — ISBN 978-1-4419-1436-1.
- ↑ 1 2 GnRH, GnRH Analogs, Gonadotropins and Gonadal Peptides. — CRC Press, 15 November 1993. — P. 455–456. — «[...] when male levels of androgens are achieved in plasma, their effects on gonadotropin secretion are similar in women and men. [...] administration of flutamide in a group of normally-cycling women produced a clinical improvement of acne and hirsutism without any significant hormonal change. [...] All these data emphasize that physiological levels of androgens have no action on the regulation of gonadotropins in normal women. [...] Androgens do not directly play a role in gonadotropin regulation [in women].». — ISBN 978-0-203-09205-7.
- ↑ Sieber PR (December 2007). "Treatment of bicalutamide-induced breast events". Expert Review of Anticancer Therapy. 7 (12): 1773—9. doi:10.1586/14737140.7.12.1773. PMID 18062751. S2CID 40410461.
- ↑ Asscheman H, Gooren LJ, Peereboom-Wynia JD (1989). "Reduction in undesired sexual hair growth with anandron in male-to-female transsexuals—experiences with a novel androgen receptor blocker". Clinical and Experimental Dermatology. 14 (5): 361—3. doi:10.1111/j.1365-2230.1989.tb02585.x. PMID 2612040. S2CID 45303518.
- ↑ Rao BR, de Voogt HJ, Geldof AA, Gooren LJ, Bouman FG (1988). "Merits and considerations in the use of anti-androgen". Journal of Steroid Biochemistry. 31 (4B): 731—7. doi:10.1016/0022-4731(88)90024-6. PMID 3143862.
- ↑ 1 2 3 Bambury RM, Scher HI (June 2015). "Enzalutamide: Development from bench to bedside". Urologic Oncology. 33 (6): 280—8. doi:10.1016/j.urolonc.2014.12.017. PMID 25797385.
- ↑ Bambury RM, Rathkopf DE (August 2016). "Novel and next-generation androgen receptor-directed therapies for prostate cancer: Beyond abiraterone and enzalutamide". Urologic Oncology. 34 (8): 348—55. doi:10.1016/j.urolonc.2015.05.025. PMID 26162486.
- ↑ 1 2 Pinto Á (February 2014). "Beyond abiraterone: new hormonal therapies for metastatic castration-resistant prostate cancer". Cancer Biology & Therapy. 15 (2): 149—55. doi:10.4161/cbt.26724. PMC 3928129. PMID 24100689.
- ↑ Orentreich N, Durr NP (July 1974). "Proceedings: Mammogenesis in transsexuals". The Journal of Investigative Dermatology. 63 (1): 142—146. doi:10.1111/1523-1747.ep12678272. PMID 4365991.
- ↑ Yen and Jaffe's Reproductive Endocrinology. — Elsevier Health Sciences, 13 September 2013. — P. 236–237. — ISBN 978-1-4557-2758-2.
- ↑ Remington and Klein's Infectious Diseases of the Fetus and Newborn Infant. — Elsevier Health Sciences, 2015. — P. 190–. — ISBN 978-0-323-24147-2.
- ↑ 1 2 Kanhai RC, Hage JJ, van Diest PJ, Bloemena E, Mulder JW (January 2000). "Short-term and long-term histologic effects of castration and estrogen treatment on breast tissue of 14 male-to-female transsexuals in comparison with two chemically castrated men". The American Journal of Surgical Pathology. 24 (1): 74—80. doi:10.1097/00000478-200001000-00009. PMID 10632490. S2CID 37752666.
- ↑ 1 2 Transgender Health Concerns // The Health of Sexual Minorities. — New York : Springer, 2006. — P. 476. — ISBN 978-0-387-28871-0. — doi:10.1007/978-0-387-31334-4_19.
- ↑ 1 2 Rosen's Breast Pathology. — 3. — Philadelphia : Lippincott Williams & Wilkins, 2009. — P. 31–. — ISBN 978-0-7817-7137-5.
- ↑ Fertility Preservation in Male Cancer Patients. — Cambridge University Press, 21 February 2013. — P. 84–. — ISBN 978-1-139-61952-3.
- ↑ Morgante E, Gradini R, Realacci M, Sale P, D'Eramo G, Perrone GA, Cardillo MR, Petrangeli E, Russo M, Di Silverio F (March 2001). "Effects of long-term treatment with the anti-androgen bicalutamide on human testis: an ultrastructural and morphometric study". Histopathology. 38 (3): 195—201. doi:10.1046/j.1365-2559.2001.01077.x. PMID 11260298. S2CID 36892099.
- ↑ 1 2 Andrology for the Clinician. — Springer Science & Business Media, 26 August 2006. — P. 76–. — ISBN 978-3-540-33713-3.
- ↑ 1 2 Testosterone: Action – Deficiency – Substitution. — Springer Science & Business Media, 6 December 2012. — P. 130, 276. — ISBN 978-3-642-72185-4.
- ↑ 1 2 Molecular Mechanisms in Spermatogenesis. — Springer Science & Business Media, 24 October 2009. — P. 258–. — ISBN 978-0-387-09597-4.
- ↑ Antiandrogens: Basic Concepts and Clinical Trials // Regulation of Male Fertility. — 1980. — P. 93–106. — ISBN 978-94-009-8877-4. — doi:10.1007/978-94-009-8875-0_10.
- ↑ 1 2 Essential Medical Physiology. — Academic Press, 14 October 2003. — P. 731–. — ISBN 978-0-08-047270-6.
- ↑ 1 2 Jones CA, Reiter L, Greenblatt E (2016). "Fertility preservation in transgender patients". International Journal of Transgenderism. 17 (2): 76—82. doi:10.1080/15532739.2016.1153992. ISSN 1553-2739. S2CID 58849546.
Traditionally, patients have been advised to cryopreserve sperm prior to starting cross-sex hormone therapy as there is a potential for a decline in sperm motility with high-dose estrogen therapy over time (Lubbert et al., 1992). However, this decline in fertility due to estrogen therapy is controversial due to limited studies.
- ↑ 1 2 The Leydig Cell in Health and Disease. — Springer Science & Business Media, 28 October 2007. — P. 422–431. — «Estrogens are highly efficient inhibitors of the hypothalamic-hypophyseal-testicular axis (212–214). Aside from their negative feedback action at the level of the hypothalamus and pituitary, direct inhibitory effects on the testis are likely (215,216). [...] The histology of the testes [with estrogen treatment] showed disorganization of the seminiferous tubules, vacuolization and absence of lumen, and compartmentalization of spermatogenesis.». — ISBN 978-1-59745-453-7.
- ↑ 1 2 Systemic Drug Treatment in Dermatology: A Handbook. — CRC Press, 1 June 2002. — P. 32–. — «[Cyproterone acetate] inhibits spermatogenesis and produces reversible infertility (but is not a male contraceptive).». — ISBN 978-1-84076-013-2.
- ↑ 1 2 Neumann F (1994). "The antiandrogen cyproterone acetate: discovery, chemistry, basic pharmacology, clinical use and tool in basic research". Exp. Clin. Endocrinol. 102 (1): 1—32. doi:10.1055/s-0029-1211261. PMID 8005205.
Spermatogenesis is also androgen-dependent and is inhibited by CPA, meaning that patients treated with high doses of CPA are sterile (Figure 23). All the effects of CPA are fully reversible.
- ↑ 1 2 Principles & Practice of Urology: A Comprehensive Text. — Universal-Publishers, 2003. — P. 684–. — «Estrogens act primarily through negative feedback at the hypothalamic-pituitary level to reduce LH secretion and testicular androgen synthesis. [...] Interestingly, if the treatment with estrogens is discontinued after 3 yr. of uninterrupted exposure, serum testosterone may remain at castration levels for up to another 3 yr. This prolonged suppression is thought to result from a direct effect of estrogens on the Leydig cells.». — ISBN 978-1-58112-412-5.
- ↑ Mast N, Lin JB, Pikuleva IA (September 2015). "Marketed Drugs Can Inhibit Cytochrome P450 27A1, a Potential New Target for Breast Cancer Adjuvant Therapy". Molecular Pharmacology. 88 (3): 428—36. doi:10.1124/mol.115.099598. PMC 4551053. PMID 26082378.
- ↑ Mast N, Zheng W, Stout CD, Pikuleva IA (February 2013). "Binding of a cyano- and fluoro-containing drug bicalutamide to cytochrome P450 46A1: unusual features and spectral response". The Journal of Biological Chemistry. 288 (7): 4613—24. doi:10.1074/jbc.M112.438754. PMC 3576067. PMID 23288837.
- ↑ Zhu Y, Liu C, Armstrong C, Lou W, Sandher A, Gao AC (September 2015). "Antiandrogens Inhibit ABCB1 Efflux and ATPase Activity and Reverse Docetaxel Resistance in Advanced Prostate Cancer". Clinical Cancer Research. 21 (18): 4133—42. doi:10.1158/1078-0432.CCR-15-0269. PMC 4573793. PMID 25995342.
- ↑ Fenner A (July 2015). "Prostate cancer: Antiandrogens reverse docetaxel resistance via ABCB1 inhibition". Nature Reviews. Urology. 12 (7): 361. doi:10.1038/nrurol.2015.135. PMID 26057062. S2CID 29729317.
- ↑ Armstrong CM, Gao AC (2015). "Drug resistance in castration resistant prostate cancer: resistance mechanisms and emerging treatment strategies". American Journal of Clinical and Experimental Urology. 3 (2): 64—76. PMC 4539108. PMID 26309896.
- ↑ 1 2 Foster WR, Car BD, Shi H, Levesque PC, Obermeier MT, Gan J, Arezzo JC, Powlin SS, Dinchuk JE, Balog A, Salvati ME, Attar RM, Gottardis MM (April 2011). "Drug safety is a barrier to the discovery and development of new androgen receptor antagonists". The Prostate. 71 (5): 480—8. doi:10.1002/pros.21263. PMID 20878947. S2CID 24620044.
- ↑ 1 2 Accounts in Drug Discovery: Case Studies in Medicinal Chemistry. — Royal Society of Chemistry, 2010. — P. 127–. — ISBN 978-1-84973-126-3.
- ↑ Kolvenbag GJ, Blackledge GR, Gotting-Smith K (January 1998). "Bicalutamide (Casodex) in the treatment of prostate cancer: history of clinical development". The Prostate. 34 (1): 61—72. doi:10.1002/(SICI)1097-0045(19980101)34:1<61::AID-PROS8>3.0.CO;2-N. PMID 9428389. S2CID 22785559.
- ↑ Blackledge GR (1996). "Clinical progress with a new antiandrogen, Casodex (bicalutamide)". Eur. Urol. 29 (Suppl 2): 96—104. doi:10.1159/000473847. PMID 8717470.
- ↑ DeVita, Hellman, and Rosenberg's Cancer: Principles & Practice of Oncology. — Wolters Kluwer Health, 7 January 2015. — P. 1142–. — ISBN 978-1-4698-9455-3.
- ↑ 1 2 Physicians' Cancer Chemotherapy Drug Manual 2013. — Jones & Bartlett Publishers, 28 December 2012. — P. 51–. — ISBN 978-1-284-04039-5.
- ↑ 1 2 Helsen C, Van den Broeck T, Voet A, Prekovic S, Van Poppel H, Joniau S, Claessens F (August 2014). "Androgen receptor antagonists for prostate cancer therapy". Endocrine-Related Cancer. 21 (4): T105-18. doi:10.1530/ERC-13-0545. PMID 24639562.
- ↑ Furr BJ (1989). ""Casodex" (ICI 176,334)--a new, pure, peripherally-selective anti-androgen: preclinical studies". Hormone Research. 32 (Suppl 1): 69—76. doi:10.1159/000181315. PMID 2533159.
- ↑ Furr BJ, Valcaccia B, Curry B, Woodburn JR, Chesterson G, Tucker H (June 1987). "ICI 176,334: a novel non-steroidal, peripherally selective antiandrogen". The Journal of Endocrinology. 113 (3): R7-9. doi:10.1677/joe.0.113R007. PMID 3625091.
- ↑ Soloway MS, Schellhammer PF, Smith JA, Chodak GW, Vogelzang NJ, Kennealey GT (December 1995). "Bicalutamide in the treatment of advanced prostatic carcinoma: a phase II noncomparative multicenter trial evaluating safety, efficacy and long-term endocrine effects of monotherapy". The Journal of Urology. 154 (6): 2110—4. doi:10.1016/S0022-5347(01)66709-0. PMID 7500470.
- ↑ Gao W, Dalton JT (March 2007). "Expanding the therapeutic use of androgens via selective androgen receptor modulators (SARMs)". Drug Discovery Today. 12 (5—6): 241—8. doi:10.1016/j.drudis.2007.01.003. PMC 2072879. PMID 17331889.
- ↑ Mason M (August 2006). "What implications do the tolerability profiles of antiandrogens and other commonly used prostate cancer treatments have on patient care?". Journal of Cancer Research and Clinical Oncology. 132 (Suppl 1): S27-35. doi:10.1007/s00432-006-0134-4. PMID 16896883. S2CID 19685819.
- ↑ Veldhuis JD, Takahashi PY, Keenan DM, Liu PY, Mielke KL, Weist SM (October 2010). "Age disrupts androgen receptor-modulated negative feedback in the gonadal axis in healthy men". Am J Physiol Endocrinol Metab. 299 (4): E675—82. doi:10.1152/ajpendo.00300.2010. PMC 2957871. PMID 20682842.
- ↑ 1 2 3 4 Foye's Principles of Medicinal Chemistry. — Lippincott Williams & Wilkins, 24 January 2012. — P. 1372–1373. — ISBN 978-1-60913-345-0.
- ↑ Essential Cancer Pharmacology: The Prescriber's Guide. — Lippincott Williams & Wilkins, 25 October 2010. — P. 49–. — ISBN 978-1-60913-704-5.
- ↑ Fradet Y (February 2004). "Bicalutamide (Casodex) in the treatment of prostate cancer". Expert Review of Anticancer Therapy. 4 (1): 37—48. doi:10.1586/14737140.4.1.37. PMID 14748655. S2CID 34153031.
In contrast, the incidence of diarrhea was comparable between the bicalutamide and placebo groups (6.3 vs. 6.4%, respectively) in the EPC program [71].
- ↑ Sharma K, Pawar GV, Giri S, Rajagopal S, Mullangi R (2012). "Development and validation of a highly sensitive LC-MS/MS-ESI method for the determination of bicalutamide in mouse plasma: application to a pharmacokinetic study". Biomedical Chromatography. 26 (12): 1589—95. doi:10.1002/bmc.2736. PMID 22495777.
- ↑ Handbook of Clinical Drug Data. — McGraw Hill Professional, 22 August 2001. — Vol. 128. — P. 245. — «With an oral dose of 50 mg/day, bicalutamide attains a peak serum level of 8.9 mg/L (21 μmol/L) 31 hr after a dose at steady state. CI of (R)-bicalutamide is 0.32 L/hr. The active (R)-enantiomer of bicalutamide is oxidized to an inactive metabolite, which, like the inactive (S)-enantiomer, is glucuronidated and cleared rapidly by elimination in the urine and feces.165». — ISBN 978-0-07-138942-6.
- ↑ 1 2 3 4 Pharmaceutical Manufacturing Encyclopedia. — 3rd. — William Andrew Publishing, 22 October 2013. — P. 627, 1695. — ISBN 978-0-8155-1856-3.
- ↑ Thin Layer Chromatography in Drug Analysis. — CRC Press, 20 December 2013. — P. 652–. — ISBN 978-1-4665-0715-9.
- ↑ Sancheti PP, Vyas VM, Shah M, Karekar P, Pore YV (2008). "Spectrophotometric estimation of bicalutamide in tablets". Indian Journal of Pharmaceutical Sciences. 70 (6): 810—2. doi:10.4103/0250-474X.49131. PMC 3040883. PMID 21369450.
- ↑ 1 2 3 4 5 Mohler ML, Bohl CE, Jones A, Coss CC, Narayanan R, He Y, Hwang DJ, Dalton JT, Miller DD (June 2009). "Nonsteroidal selective androgen receptor modulators (SARMs): dissociating the anabolic and androgenic activities of the androgen receptor for therapeutic benefit". Journal of Medicinal Chemistry. 52 (12): 3597—617. doi:10.1021/jm900280m. PMID 19432422.
[C]linically relevant antiandrogens currently are nonsteroidal anilide derivatives. Antiandrogens used for prostate cancer include the monoarylpropionamide flutamide (1) (a prodrug of hydroxyflutamide (2)),29–31 the hydantoin nilutamide(3),32–34 and the diarylpropionamide bicalutamide (4) (Chart1).35–37
- ↑ 1 2 Bioorganic and Medicinal Chemistry of Fluorine. — John Wiley & Sons, 2 June 2008. — P. 327–. — ISBN 978-0-470-28187-1.
- ↑ Ball AL, Kamalian L, Alfirevic A, Lyon JJ, Chadwick AE (July 2016). "Identification of the Additional Mitochondrial Liabilities of 2-Hydroxyflutamide When Compared With its Parent Compound, Flutamide in HepG2 Cells". Toxicological Sciences. 153 (2): 341—351. doi:10.1093/toxsci/kfw126. PMC 5036617. PMID 27413113.
- ↑ 1 2 Hermkens PH, Kamp S, Lusher S, Veeneman GH (July 2006). "Non-steroidal steroid receptor modulators". IDrugs. 9 (7): 488—94. doi:10.2174/0929867053764671. PMID 16821162.
- ↑ Hair Transplantation. — Cambridge University Press, 30 November 2009. — P. 11–. — ISBN 978-1-139-48339-1.
- ↑ Hair Transplantation. — Elsevier Health Sciences, 2006. — P. 6–7. — ISBN 978-1-4160-3104-8.
- ↑ Kawahara T, Minamoto H (2014). "Androgen Receptor Antagonists in the Treatment of Prostate Cancer". Clinical Immunology, Endocrine & Metabolic Drugs. 1 (1): 11—19. doi:10.2174/22127070114019990002.
- ↑ Moilanen AM, Riikonen R, Oksala R, Ravanti L, Aho E, Wohlfahrt G, Nykänen PS, Törmäkangas OP, Palvimo JJ, Kallio PJ (2015). "Discovery of ODM-201, a new-generation androgen receptor inhibitor targeting resistance mechanisms to androgen signaling-directed prostate cancer therapies". Sci Rep. 5: 12007. Bibcode:2015NatSR...512007M. doi:10.1038/srep12007. PMC 4490394. PMID 26137992.
- ↑ 1 2 3 Segal S, Narayanan R, Dalton JT (April 2006). "Therapeutic potential of the SARMs: revisiting the androgen receptor for drug discovery". Expert Opinion on Investigational Drugs. 15 (4): 377—87. doi:10.1517/13543784.15.4.377. PMID 16548787. S2CID 31787187.
Structural modifications of bicalutamide led to the discovery of the first nonsteroidal androgens (the aryl propionamides) in 1998. Lead compounds in this class (denoted S1 and S4 in published literature) not only bind to the AR with high affinity (low nanomolar range), but also demonstrate tissue selectivity in animal models [46,50].
- ↑ Yin D, Gao W, Kearbey JD, Xu H, Chung K, He Y, Marhefka CA, Veverka KA, Miller DD, Dalton JT (March 2003). "Pharmacodynamics of selective androgen receptor modulators". The Journal of Pharmacology and Experimental Therapeutics. 304 (3): 1334—40. doi:10.1124/jpet.102.040840. PMC 2040238. PMID 12604714.
- ↑ Nuclear Receptors as Drug Targets. — John Wiley & Sons, 8 September 2008. — P. 257–258. — ISBN 978-3-527-62330-3.
- ↑ 1 2 3 4 Parent EE, Dence CS, Jenks C, Sharp TL, Welch MJ, Katzenellenbogen JA (2007). "Synthesis and biological evaluation of [18F]bicalutamide, 4-[76Br]bromobicalutamide, and 4-[76Br]bromo-thiobicalutamide as non-steroidal androgens for prostate cancer imaging". J. Med. Chem. 50 (5): 1028—40. doi:10.1021/jm060847r. PMID 17328524.
- ↑ 1 2 3 PET and SPECT of Neurobiological Systems. — Springer Science & Business Media, 15 February 2014. — P. 394–. — ISBN 978-3-642-42014-6.
- ↑ 1 2 de Jesus Cortez F, Nguyen P, Truillet C, Tian B, Kuchenbecker KM, Evans MJ, Webb P, Jacobson MP, Fletterick RJ, England PM (2017). "Development of 5N-Bicalutamide, a High-Affinity Reversible Covalent Antiandrogen". ACS Chem. Biol. 12 (12): 2934—2939. doi:10.1021/acschembio.7b00702. PMID 28981251. S2CID 24974359.
- ↑ England, Pamela M.; Fletterick, R. J. & Kuchenbecker, K. et al., US Patent 10053433B2, published 2016
- ↑ 1 2 Tucker H, Crook JW, Chesterson GJ (1988). "Nonsteroidal antiandrogens. Synthesis and structure-activity relationships of 3-substituted derivatives of 2-hydroxypropionanilides". Journal of Medicinal Chemistry. 31 (5): 954—9. doi:10.1021/jm00400a011. PMID 3361581.
- ↑ James KD, Ekwuribe NN (2002). "A Two-step Synthesis of the Anti-cancer Drug (R,S)-Bicalutamide". Synthesis. 2002 (7): 850—2. doi:10.1055/s-2002-28508.
- ↑ Pizzetti E, Vigano E, Lussana M, Landonio E, "Procedure for the synthesis of bicalutamide", US application 2006/0041161, published 23 February 2006 Архивировано {{{2}}}.
- ↑ Diamanti-Kandarakis E (September 1999). "Current aspects of antiandrogen therapy in women". Current Pharmaceutical Design. 5 (9): 707—23. doi:10.2174/1381612805666230111201150. PMID 10495361. Архивировано 10 января 2023. Дата обращения: 27 сентября 2016.
Several trials demonstrated complete clearing of acne with flutamide [62,77]. Flutamide used in combination with an [oral contraceptive], at a dose of 500mg/d, flutamide caused a dramatic decrease (80%) in total acne, seborrhea and hair loss score after only 3 months of therapy [53]. When used as a monotherapy in lean and obese PCOS, it significantly improves the signs of hyperandrogenism, hirsutism and particularly acne [48]. [...] flutamide 500mg/d combined with an [oral contraceptive] caused an increase in cosmetically acceptable hair density, in sex of seven women suffering from diffuse androgenetic alopecia [53].
- ↑ Textbook of Prostate Cancer: Pathology, Diagnosis and Treatment: Pathology, Diagnosis and Treatment. — CRC Press, 1 March 1999. — P. 55,279–280. — ISBN 978-1-85317-422-3.
- ↑ The Dictionary of Drugs: Chemical Data: Chemical Data, Structures and Bibliographies. — Springer, 14 November 2014. — P. 573–. — ISBN 978-1-4757-2085-3.
- ↑ Furr BJ (1998). "Research on reproductive medicine in the pharmaceutical industry". Hum Fertil (Camb). 1 (1): 56—63. doi:10.1080/1464727982000198131. PMID 11844311.
- ↑ Cadilla R, Turnbull P (2006). "Selective androgen receptor modulators in drug discovery: medicinal chemistry and therapeutic potential". Curr Top Med Chem. 6 (3): 245—70. doi:10.2174/156802606776173456. PMID 16515480. Архивировано 18 августа 2020. Дата обращения: 11 декабря 2019.
- ↑ Pharmaceutical Substances: Syntheses, Patents and Applications of the most relevant APIs. — 5th. — Thieme, 2009. — P. 153–154. — ISBN 978-3-13-179275-4.
- ↑ Furr BJ, Valcaccia B, Curry B, Woodburn JR, Chesterson G, Tucker H (June 1987). "ICI 176,334: a novel non-steroidal, peripherally selective antiandrogen". The Journal of Endocrinology. 113 (3): R7-9. doi:10.1677/joe.0.113r007. PMID 3625091.
- ↑ Newling DW (1990). "The response of advanced prostatic cancer to a new non-steroidal antiandrogen: results of a multicenter open phase II study of Casodex. European/Australian Co-operative Group". European Urology. 18 (Suppl 3): 18—21. doi:10.1159/000463973. PMID 2094607.
- ↑ The United States Patents Quarterly. — Associated Industry Publications, 1997.
- ↑ Chaurasiya A, Singh AK, Upadhyay SC, Asati D, Ahmad FJ, Mukherjee R, Khar (2012). "Lipidic Nanocarrier for Oral Bioavailability Enhancement of an Anticancer Agent: Formulation Design and Evaluation". Advanced Science Letters. 11 (1): 43—52. doi:10.1166/asl.2012.2170. ISSN 1936-6612.
- ↑ Klotz L (May 2006). "Combined androgen blockade: an update". The Urologic Clinics of North America. 33 (2): 161—6, v—vi. doi:10.1016/j.ucl.2005.12.001. PMID 16631454.
- ↑ Gohil K (August 2015). "Exciting Therapies Ahead in Prostate Cancer". P & T. 40 (8): 530—531. PMC 4517537. PMID 26236143.
- ↑ Kolvenbag GJ, Iversen P, Newling DW (2001). "Antiandrogen monotherapy: a new form of treatment for patients with prostate cancer". Urology. 58 (2 Suppl 1): 16—23. doi:10.1016/s0090-4295(01)01237-7. PMID 11502439.
- ↑ Carswell CI, Figgitt DP (2002). "Bicalutamide: in early-stage prostate cancer". Drugs. 62 (17): 2471—79, discussion 2480–1. doi:10.2165/00003495-200262170-00006. PMID 12421104. S2CID 195690919.
- ↑ Textbook of Bone Metastases. — John Wiley & Sons, 27 September 2005. — P. 493–. — ISBN 978-0-470-01160-7.
- ↑ United Nations. Consolidated List of Products Whose Consumption And/or Sale Have Been Banned, Withdrawn, Severely Restricted Or Not Approved by Governments: Pharmaceuticals. — United Nations Publications, 2005. — P. 4–. — ISBN 978-92-1-130241-7.
- ↑ Bono AV (2004). "Overview of Current Treatment Strategies in Prostate Cancer". European Urology Supplements. 3 (1): 2—7. doi:10.1016/j.eursup.2003.12.002.
The Canadian Health Authorities have withdrawn the approval for antiandrogen monotherapy with bicalutamide for the treatment of localised prostate cancer [5]. Several European countries have also withdrawn approval for bicalutamide for this indication.
- ↑ 1 2 Moul JW (August 2009). "Twenty years of controversy surrounding combined androgen blockade for advanced prostate cancer". Cancer. 115 (15): 3376—8. doi:10.1002/cncr.24393. PMID 19484788. S2CID 5670663.
- ↑ Dx/Rx: Prostate Cancer. — Jones & Bartlett Publishers, 20 March 2012. — P. 178–. — ISBN 978-0-7637-9453-8.
- ↑ Cancer and its Management. — Wiley, 3 October 2014. — P. 379–. — ISBN 978-1-118-46871-5.
- ↑ Tumours in Urology. — Springer Science & Business Media, 1994. — P. 233–. — ISBN 978-1-4471-2086-5.
- ↑ Sex and Gender Differences in Pharmacology. — Springer Science & Business Media, 2 October 2012. — P. 575–. — ISBN 978-3-642-30725-6.
- ↑ Bohl CE, Gao W, Miller DD, Bell CE, Dalton JT (April 2005). "Structural basis for antagonism and resistance of bicalutamide in prostate cancer". Proceedings of the National Academy of Sciences of the United States of America. 102 (17): 6201—6. Bibcode:2005PNAS..102.6201B. doi:10.1073/pnas.0500381102. PMC 1087923. PMID 15833816.
- ↑ Kolinsky M, de Bono JS (2016). "The Ongoing Challenges of Targeting the Androgen Receptor". European Urology. 69 (5): 841—3. doi:10.1016/j.eururo.2015.10.052. PMID 26585581. Архивировано 20 сентября 2016. Дата обращения: 9 сентября 2016.
- ↑ 1 2 Concise Dictionary of Pharmacological Agents: Properties and Synonyms. — Springer Science & Business Media, 6 December 2012. — P. 51–. — ISBN 978-94-011-4439-1.
- ↑ Dictionary of Pharmacological Agents. — CRC Press, 21 November 1996. — P. 570–. — ISBN 978-0-412-46630-4.
- ↑ (Report) https://www.who.int/medicines/services/inn/StemBook_2013_Final.pdf.
{{cite report}}:|title=пропущен или пуст (справка)Википедия:Обслуживание CS1 (url-status) (ссылка) - ↑ 21 results for Name/Synonym ends with LUTAMIDE. Drug Information Portal. Дата обращения: 19 ноября 2017. Архивировано 27 июля 2020 года.
- ↑ Parallel Genetic Algorithms for Crystal Structure Prediction: Successes and Failures in Predicting Bicalutamide Polymorphs // Emerging Intelligent Computing Technology and Applications: 5th International Conference on Intelligent Computing, ICIC 2009 Ulsan, South Korea, September 16–19, 2009 Proceedings. — Springer, 19 September 2009. — Vol. 5754. — P. 120–. — ISBN 978-3-642-04070-2. — doi:10.1007/978-3-642-04070-2_14.
- ↑ Dhas NL, Ige PP, Kudarha RR (2015). "Design, optimization and in-vitro study of folic acid conjugated-chitosan functionalized PLGA nanoparticle for delivery of bicalutamide in prostate cancer". Powder Technology. 283: 234—245. doi:10.1016/j.powtec.2015.04.053.
- ↑ Ramadan WH, Kabbara WK, Al Basiouni Al Masri HS (2015). "Enzalutamide for patients with metastatic castration-resistant prostate cancer". OncoTargets and Therapy. 8: 871—6. doi:10.2147/OTT.S80488. PMC 4407758. PMID 25945058.
- ↑ 1 2 Understanding Pharmacology for Pharmacy Technicians. — ASHP, 2 April 2013. — P. 268–. — ISBN 978-1-58528-360-6.
- ↑ 1 2 Allan GF, Sui Z (2003). "Therapeutic androgen receptor ligands". Nucl Recept Signal. 1: e009. doi:10.1621/nrs.01009. PMC 1402218. PMID 16604181.
- ↑ Emans, Laufer, Goldstein's Pediatric and Adolescent Gynecology. — Lippincott Williams & Wilkins, 5 January 2012. — P. 365–. — «Therapy with GnRH analogs is expensive and requires intramuscular injections of depot formulations, the insert of a subcutaneous implant yearly, or, much less commonly, daily subcutaneous injections.». — ISBN 978-1-4511-5406-1.
- ↑ Practical Pediatric and Adolescent Gynecology. — John Wiley & Sons, 29 March 2013. — P. 182–. — «Treatment is expensive, with costs typicall in the range of $10,000–$15,000 per year.». — ISBN 978-1-118-53857-9.
- ↑ 1 2 3 Annual Report and Form 20-F 2007. AstraZeneca.
- ↑ 1 2 Actavis Generic Prostate Cancer Drug Bicalutamide First to Market in UK, Germany, France. Press Release. AstraZeneca, Actavis (10 июля 2008).
- ↑ 1 2 "Hormonal Therapies" (PDF). Future Oncology. 2 (2—3): 306. June 1996. Архивировано из оригинала (PDF) 9 сентября 2017. Дата обращения: 1 июля 2017.
- ↑ 1 2 Zeneca of Britain Posts Strong Drug Profits. The New York Times (12 марта 1997).
- ↑ 1 2 Annual Report and Form 20-F 2001. AstraZeneca.
- ↑ 1 2 Annual Report and Form 20-F 2004. AstraZeneca.
- ↑ 1 2 Annual Report and Form 20-F 2010. AstraZeneca.
- ↑ 1 2 Annual Report and Form 20-F 2013. AstraZeneca.
- ↑ 1 2 Annual Report and Form 20-F 2016. AstraZeneca. Архивировано 3 апреля 2017 года.
- ↑ 1 2 AstraZeneca Full-Year 2017 Results. AstraZeneca.
- ↑ 1 2 AstraZeneca Full-Year 2018 Results. AstraZeneca.
- ↑ Pharmacology and Therapeutics for Dentistry. — Elsevier Health Sciences, 19 March 2010. — P. 851–. — ISBN 978-0-323-07824-5.
- ↑ Preventing Medication Errors and Improving Drug Therapy Outcomes: A Management Systems Approach. — CRC Press, 25 February 2003. — P. 136–137. — ISBN 978-0-203-01073-0.
- ↑ Responsibility for Drug-induced Injury: A Reference Book for Lawyers, the Health Professions and Manufacturers. — IOS Press, January 1998. — P. 241–8. — ISBN 978-90-5199-387-5.
- ↑ Wang LG, Mencher SK, McCarron JP, Ferrari AC (2004). "The biological basis for the use of an anti-androgen and a 5-alpha-reductase inhibitor in the treatment of recurrent prostate cancer: Case report and review". Oncology Reports. 11 (6): 1325—9. doi:10.3892/or.11.6.1325. PMID 15138573.
- ↑ Tay MH, Kaufman DS, Regan MM, Leibowitz SB, George DJ, Febbo PG, Manola J, Smith MR, Kaplan ID, Kantoff PW, Oh WK (2004). "Finasteride and bicalutamide as primary hormonal therapy in patients with advanced adenocarcinoma of the prostate". Annals of Oncology. 15 (6): 974—8. doi:10.1093/annonc/mdh221. PMID 15151957.
- ↑ Merrick GS, Butler WM, Wallner KE, Galbreath RW, Allen ZA, Kurko B (2006). "Efficacy of neoadjuvant bicalutamide and dutasteride as a cytoreductive regimen before prostate brachytherapy". Urology. 68 (1): 116—20. doi:10.1016/j.urology.2006.01.061. PMID 16844453.
- ↑ Sartor O, Gomella LG, Gagnier P, Melich K, Dann R (2009). "Dutasteride and bicalutamide in patients with hormone-refractory prostate cancer: the Therapy Assessed by Rising PSA (TARP) study rationale and design". The Canadian Journal of Urology. 16 (5): 4806—12. PMID 19796455.
- ↑ Chu FM, Sartor O, Gomella L, Rudo T, Somerville MC, Hereghty B, Manyak MJ (2015). "A randomised, double-blind study comparing the addition of bicalutamide with or without dutasteride to GnRH analogue therapy in men with non-metastatic castrate-resistant prostate cancer". European Journal of Cancer. 51 (12): 1555—69. doi:10.1016/j.ejca.2015.04.028. PMID 26048455.
- ↑ Gaudet M, Vigneault É, Foster W, Meyer F, Martin AG (2016). "Randomized non-inferiority trial of Bicalutamide and Dutasteride versus LHRH agonists for prostate volume reduction prior to I-125 permanent implant brachytherapy for prostate cancer". Radiotherapy and Oncology. 118 (1): 141—7. doi:10.1016/j.radonc.2015.11.022. PMID 26702991.
- ↑ Dijkstra S, Witjes WP, Roos EP, Vijverberg PL, Geboers AD, Bruins JL, Smits GA, Vergunst H, Mulders PF (2016). "The AVOCAT study: Bicalutamide monotherapy versus combined bicalutamide plus dutasteride therapy for patients with locally advanced or metastatic carcinoma of the prostate-a long-term follow-up comparison and quality of life analysis". SpringerPlus. 5: 653. doi:10.1186/s40064-016-2280-8. PMC 4870485. PMID 27330919.
- ↑ Fujimura T, Takayama K, Takahashi S, Inoue S (January 2018). "Estrogen and Androgen Blockade for Advanced Prostate Cancer in the Era of Precision Medicine". Cancers. 10 (2): 29. doi:10.3390/cancers10020029. PMC 5836061. PMID 29360794.
- ↑ Ho TH, Nunez-Nateras R, Hou YX, Bryce AH, Northfelt DW, Dueck AC, et al. (April 2017). "A Study of Combination Bicalutamide and Raloxifene for Patients With Castration-Resistant Prostate Cancer". Clinical Genitourinary Cancer. 15 (2): 196—202.e1. doi:10.1016/j.clgc.2016.08.026. PMID 27771244. S2CID 19043552.
- ↑ Translational Breast Cancer Research Consortium (TBCRC) (2012). "Targeting the androgen receptor (AR) in women with AR+ ER-/PR- metastatic breast cancer (MBC)". J Clin Oncol (suppl): abstract 1006. Архивировано 10 июля 2015.
- ↑ Clinical trial number NCT00468715 for "Bicalutamide in Treating Patients With Metastatic Breast Cancer" at ClinicalTrials.gov
- ↑ Gucalp A, Tolaney S, Isakoff SJ, Ingle JN, Liu MC, Carey LA, Blackwell K, Rugo H, Nabell L, Forero A, Stearns V, Doane AS, Danso M, Moynahan ME, Momen LF, Gonzalez JM, Akhtar A, Giri DD, Patil S, Feigin KN, Hudis CA, Traina TA (October 2013). "Phase II trial of bicalutamide in patients with androgen receptor-positive, estrogen receptor-negative metastatic Breast Cancer". Clinical Cancer Research. 19 (19): 5505—12. doi:10.1158/1078-0432.CCR-12-3327. PMC 4086643. PMID 23965901.
- ↑ Caiazza F, Murray A, Madden SF, Synnott NC, Ryan EJ, O'Donovan N, Crown J, Duffy MJ (April 2016). "Preclinical evaluation of the AR inhibitor enzalutamide in triple-negative breast cancer cells". Endocrine-Related Cancer. 23 (4): 323—34. doi:10.1530/ERC-16-0068. PMID 26932782.
- ↑ Traina TA, et al. (2015). "Results from a phase 2 study of enzalutamide (ENZA), an androgen receptor (AR) inhibitor, in advanced AR+ triple-negative breast cancer (TNBC)". Journal of Clinical Oncology. 33 (suppl): abstr 1003. doi:10.1200/jco.2015.33.15_suppl.1003. Архивировано 30 мая 2016.
- ↑ Levine D, Park K, Juretzka M, Esch J, Hensley M, Aghajanian C, Lewin S, Konner J, Derosa F, Spriggs D, Iasonos A, Sabbatini P (December 2007). "A phase II evaluation of goserelin and bicalutamide in patients with ovarian cancer in second or higher complete clinical disease remission". Cancer. 110 (11): 2448—56. doi:10.1002/cncr.23072. PMID 17918264. S2CID 21161915.
- ↑ 1 2 3 Principles and Practice of Endocrinology and Metabolism. — Lippincott Williams & Wilkins, 2001. — P. 1209. — ISBN 978-0-7817-1750-2.
- ↑ 1 2 3 4 Lepor H (1993). "Medical therapy for benign prostatic hyperplasia". Urology. 42 (5): 483—501. doi:10.1016/0090-4295(93)90258-c. PMID 7694413.
The clinically significant adverse events reported in the casodex group included breast tenderness (93%), breast enlargement (54%), and sexual dysfunction (60%). In none of the patients in the placebo group did any of these adverse events develop. None of the subjects discontinued therapy owing to an adverse event.
- ↑ Lee M, Sharifi R (1997). "Benign prostatic hyperplasia: diagnosis and treatment guideline". Ann Pharmacother. 31 (4): 481—6. doi:10.1177/106002809703100415. PMID 9101011. S2CID 20498549.
- ↑ Kenny B, Ballard S, Blagg J, Fox D (1997). "Pharmacological options in the treatment of benign prostatic hyperplasia". J. Med. Chem. 40 (9): 1293—315. doi:10.1021/jm960697s. PMID 9135028.
- ↑ McCoy J, Wambier CG, Vano-Galvan S, Shapiro J, Sinclair R, Müller Ramos P, Washenik K, Andrade M, Herrera S, Goren A (April 2020). "Racial Variations in COVID-19 Deaths May Be Due to Androgen Receptor Genetic Variants Associated with Prostate Cancer and Androgenetic Alopecia. Are Anti-Androgens a Potential Treatment for COVID-19?". J Cosmet Dermatol. 19 (7): 1542—1543. doi:10.1111/jocd.13455. PMC 7267367. PMID 32333494.
- ↑ A Phase II Trial to Promote Recovery from COVID-19 with Endocrine Therapy (2 марта 2021).
- ↑ Kirk's Current Veterinary Therapy XV. — Elsevier Health Sciences, 1 December 2013. — P. 908. — ISBN 978-0-323-22762-9.
- ↑ Manual of Exotic Pet Practice. — Elsevier Health Sciences, 2009. — P. 363. — ISBN 978-1-4160-0119-5.
- ↑ 1 2 Endocrinology, An Issue of Veterinary Clinics: Exotic Animal Practice. — Elsevier Health Sciences, 9 February 2014. — P. 16–17. — «In ferrets, 5 mg/kg [of bicalutamide] orally every 24 hours has been used clinically, but no controlled toxicologic or pharmacologic studies have been published at this time.». — ISBN 978-0-323-26419-8.
- ↑ Biology and Diseases of the Ferret. — Wiley, 26 March 2014. — P. 980. — «Other agents have been proposed for medical management of [adrenal-associated endocrinopathy] but have not been studied. Possibly medications include the androgen receptor blockers flutamide and bicalutamide, the anti-androgen finasteride, estrogen-inhibiting anastrozole, and another GnRH analog, goserelin. [...] None of these drugs have been tested in controlled clinical trials in ferrets.». — ISBN 978-1-118-78273-6.
Дальнейшее чтение[править | править код]
[[Категория:Ветеринарные препараты]] [[Категория:Гепатотоксины]] [[Категория:Удаление волос]] [[Категория:Антигестагены]] [[Категория:Анилиды]] [[Категория:Страницы с непроверенными переводами]]