Финастерид
| Финастерид | |
|---|---|
| Finasteride | |
 | |
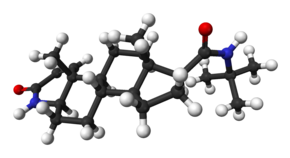 | |
| Химическое соединение | |
| ИЮПАК | N-трет-Бутил-3-оксо-4-аза-5альфа-андрост-1-ен-17бета-карбоксамид |
| Брутто-формула | C23H36N2O2 |
| Молярная масса | 372.549 г/моль |
| CAS | 98319-26-7 |
| PubChem | 194453 |
| DrugBank | APRD00632 |
| Состав | |
| Классификация | |
| АТХ | G04CB01, D11AX10 |
| Фармакокинетика | |
| Биодоступн. | 63% |
| Метаболизм | Hepatic |
| Период полувывед. |
Elderly: 8 часов Adults: 6 часов |
| Экскреция | Feces (57%) and urine (39%) as metabolites |
| Лекарственные формы | |
| таблетки покрытые оболочкой, таблетки покрытые пленочной оболочкой | |
| Способы введения | |
| Oral | |
| Другие названия | |
| Альфинал, Зерлон, Пенестер, Проскар, Простерид®, Финаст®, Финастерид, Финпрос | |
Финастерид — лекарственное средство, противоопухолевый препарат, применяемый при лечении доброкачественной гиперплазии предстательной железы (аденомы простаты) и облысения у мужчин.
История
[править | править код]В 1942 году Джеймс Гамильтон заметил, что кастрация в препубертатном возрасте предотвращает дальнейшее развитие облысения у зрелых мужчин[1]. В 1974 году Джулианна Императо-МакГинли из Корнеллского медицинского колледжа в Нью-Йорке приняла участие в медицинской конференции, где она сообщила о группе интерсекс-детей на Антильских островах, которые от рождения имели гениталии промежуточного типа и воспитывались как девочки, но после наступления половой зрелости у них выросли внешние мужские гениталии и другие мужские признаки. Местные жители называли их «гуэведосе», что на испанском языке означает «пенис в двенадцать». Её исследовательская группа обнаружила, что у этих детей была генетическая мутация, вызывающая дефицит фермента 5α-редуктазы и мужского гормона дигидротестостерона (DHT), который был причиной отклонений в половом развитии мужчин. После полового созревания у таких людей наблюдается уменьшенная в размерах, недоразвитая предстательная железа, а также отсутствие случаев облысения у мужчин[2][3].
В 1975 году копии презентации Императо-МакГинли увидели Рой Вагелос, который тогда работал руководителем по фундаментальным исследованиям в фармакологической компании Мерк и Ко. Он был заинтригован тем, что снижение уровня DHT приводит к развитию более маленькой простаты. Затем доктор Вагелос попытался создать лекарство, которое могло бы имитировать состояние, которое встречается у таких детей, для лечения пожилых мужчин, страдающих доброкачественной гиперплазией предстательной железы[4].
Финастерид был разработан Merck под кодовым названием MK-906[5]. В 1992 году финастерид (5 мг) был одобрен Управлением по санитарному надзору за качеством пищевых продуктов и медикаментов США (FDA) для лечения ДГПЖ, который Мерк и Ко продавал под торговой маркой Proscar. В 1997 году Мерк и Ко удалось получить одобрение FDA для второго показания к финастериду (1 мг) для лечения выпадения волос по мужскому типу, который продавался под торговой маркой Propecia[6]. Это был первый введенный ингибитор 5α-редуктазы, за которым последовал дутастерид в 2001 году[7]. Первое исследование финастерида в лечении гирсутизма у женщин было опубликовано в 1994 году[8]. Известно, что бывший президент США Дональд Трамп принимает финастерид («Пропецию») в качестве средства против облысения[9].
Фармакологическое действие
[править | править код]Ингибирует 5-альфа-редуктазу II типа, превращающую тестостерон в более активный 5-альфа-дигидротестостерон, снижает его концентрацию в крови и ткани предстательной железы в течение 24 ч после перорального приема. Угнетает стимулирующее действие тестостерона на развитие опухоли. Подавление образования дигидротестостерона сопровождается уменьшением объема предстательной железы, увеличением максимальной скорости тока мочи и уменьшением симптомов непроходимости мочевыводящих путей. При постоянном приеме статистически значимый эффект регистрируется через 3 мес (уменьшение объема железы), 4 мес (увеличение максимальной скорости тока мочи) и 7 мес (уменьшение общих симптомов и симптомов непроходимости мочевыводящих путей). При прекращении приёма препарата, изменения предстательной железы восстанавливаются в течение 6-8 месяцев.
Рак простаты
[править | править код]Результаты, проведенных в 2005 году исследований в Национальном институте рака (США) показали, что при приёме 5 мг в день, как это обычно назначают при ДГПЖ, у участников исследований, принимавших финастерид, случаи появления рака простаты были на 25% меньше в конце исследования по сравнению с пациентами, получавшими плацебо.
Фармакокинетика
[править | править код]Абсорбция в желудочно-кишечном тракте завершается через 6—8 ч после приема. Хорошо всасывается и проникает в ткани и биожидкости, обнаруживается в эякуляте (в концентрации 5 мкг). Биодоступность — 80%, не зависит от приема пищи. TCmax — 2 ч, Cmax — 8—10 нг/мл. Связь с белками плазмы — 93%. Проникает через ГЭБ (через 7—10 дней лечения обнаруживается в спинномозговой жидкости в незначительных количествах) Системный клиренс — 165 мл/мин, объем распределения — 76 л. Незначительно кумулирует при длительном приеме. T½ у мужчин 18—60 лет — 6 ч, у мужчин старше 70 лет — 8 ч. Выводится в виде метаболитов почками (39%) и через кишечник (57%). При хронической почечной недостаточности часть метаболитов (которая в норме выводится с мочой) выводится с калом.
Показания
[править | править код]Доброкачественная гиперплазия предстательной железы (для уменьшения размеров предстательной железы, увеличение максимальной скорости оттока мочи, снижение риска развития острой задержки мочи).
Также применяется для лечения андрогенетической алопеции.
Противопоказания
[править | править код]В разделе не хватает ссылок на источники (см. рекомендации по поиску). |
Гиперчувствительность, беременность, женщины детородного возраста, детский возраст.
C осторожностью
[править | править код]Печеночная недостаточность, обструктивная уропатия.
Режим дозирования
[править | править код]Внутрь, независимо от приема пищи, по 5 мг 1 раз в день, как в монотерапии, так и в сочетании с доксазозином.
Побочные эффекты
[править | править код]В разделе не хватает ссылок на источники (см. рекомендации по поиску). |
Аллергические реакции (сыпь, кожный зуд, крапивница, отёк губ и лица), снижение потенции и/или либидо, нарушение эякуляции, уменьшение объема эякулята, увеличение и болезненность молочных желёз, повышение концентрации лютеинизирующего гормона и фолликулостимулирующего гормона в крови, снижение концентрации простат-специфического антигена (ПСА).
Особые указания
[править | править код]У пациентов с большим объёмом остаточной мочи и/или резко сниженным током мочи необходим тщательный контроль возможного развития обструктивной уропатии. Перед началом терапии необходимо исключить заболевания, симулирующие доброкачественную гиперплазию предстательной железы, — рак предстательной железы, стриктура уретры, гипотония мочевого пузыря, нарушения его иннервации и инфекционный простатит. Женщинам детородного возраста и беременным следует избегать контакта с препаратом, он обладает тератогенными свойствами (способность подавлять превращение тестостерона в дигидротестостерон может вызывать нарушение развития половых органов у плода мужского пола), проникает в семенную жидкость. Вызывает снижение простат-специфического антигена через 6 и 12 месяцев приёма на 41 и 48% соответственно. Для исключения развития рака предстательной железы во время терапии финастеридом необходимы обследования пациентов.
Примечания
[править | править код]- ↑ Hamilton, J (1942). «Male hormone stimulation is prerequisite and an incitant in common baldness». American Journal of Anatomy. 71 (3): 451—480. doi:10.1002/aja.1000710306
- ↑ Imperato-McGinley J, Guerrero L, Gautier T, Peterson RE (December 1974). «Steroid 5alpha-reductase deficiency in man: an inherited form of male pseudohermaphroditism». Science. 186 (4170): 1213-5. doi:10.1126/science.186.4170.1213. PMID 4432067
- ↑ Isfort AH, Emerick JE, Paz RA (11 November 2016). «5-Alpha-Reductase Deficiency». WebMD. News & Perspective Drugs & Diseases CME & Education Academy Consult, Drugs & Diseases > Pediatrics: General Medicine.
- ↑ Freudenheim M (February 16, 1992). «Keeping the Pipeline Filled at Merck». The New York Times
- ↑ Sudduth SL, Koronkowski MJ (1993). «Finasteride: the first 5α-reductase inhibitor». Pharmacotherapy. 13 (4): 309-25, discussion 325-9. doi:10.1002/j.1875-9114.1993.tb02739.x (inactive 2019-07-04). PMID 7689728
- ↑ Alfred Burger, Donald J. Abraham. Burger's Medicinal Chemistry and Drug Discovery, Autocoids, Diagnostics, and Drugs from New Biology. — Wiley, 2003-02-20. — 732 с. — ISBN 9780471370307. Архивировано 10 января 2023 года.
- ↑ Annette M. Doherty. Annual Reports in Medicinal Chemistry. — Academic Press, 2003-09-24. — 484 с. — ISBN 9780120405381. Архивировано 10 января 2023 года.
- ↑ Diamanti-Kandarakis E, Tolis G, Duleba AJ (1995). «Androgens and therapeutic aspects of antiandrogens in women». J. Soc. Gynecol. Investig. 2 (4): 577-92. doi:10.1177/107155769500200401. PMID 9420861
- ↑ Источник. Дата обращения: 28 января 2020. Архивировано 19 ноября 2019 года.